下列混合物的除杂方法与发生反应的类型均正确的是
| |
混合物 |
加入试剂或方法 |
反应类型 |
| A |
除去O2中的CO |
通入炽热的CuO中 |
化合反应 |
| B |
除去CO2中的HCl |
通入饱和NaHCO3溶液中 |
中和反应 |
| C |
除去CaCO3中的Na2CO3 |
溶解、加入BaCl2溶液 |
复分解反应 |
| D |
除去NaCl中的Na2CO3 |
加入适量盐酸、蒸发 |
复分解反应 |
Al、Fe、Cu都是重要的金属元素,下列说法正确的是
| A.铝的氧化物粉末是白色的,属于两性氧化物;铁、铜的最高价氧化物粉末都是黑色的,属于碱性氧化物 |
| B.铝制品、铁制品、铜制品长期放置在空气中均易腐蚀 |
| C.制备AlCl3、FeCl3、CuCl2均能采用单质与氯气反应的方法 |
| D.常温下Cu、Fe、Al均不能和浓硫酸发生化学反应 |
甲、乙、丙、丁四种元素位于同一短周期,原子序数依次增加。下列判断错误的是
| A.原子半径:丙<乙<甲 |
| B.若甲、乙、丙、丁的单质在常温下均为气态,则核电荷数比甲少1的元素形成的单质熔点可能很高。 |
| C.若甲、乙、丙均是金属,则氢氧化物碱性:甲<乙<丙 |
| D.若乙的最高价含氧酸为强酸,则丙是活泼非金属元素 |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
| B.53gNa2CO3固体含有的CO32-离子数为0.5 NA |
| C.室温下,21.0g乙烯和丁烯的混合气体中含有的共价键数目为3NA |
| D.5.6 g Fe和一定量的浓HNO3或稀HNO3完全反应,转移电子一定均为0.3NA |
下列说法正确的是:
| A.某烷烃的系统命名:3-甲基-2-乙基戊烷 |
| B.氨基乙酸和硝基乙烷互为同分异构体 |
| C.乙烯和1,3-丁二烯属于同系物 |
D.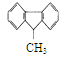 一氯代物有5种 一氯代物有5种 |
下列说法正确的是
A.由C、H、O、N四种元素组成的化合物一定是离子化合物
B.ⅠA族除氢元素外的所有元素的金属性比ⅡA族元素的金属性强
C.含有最高价元素的化合物不一定具有很强的氧化性
D.化学键存在于原子之间,也存在于分子之间