下列关于物质或离子检验的叙述正确的是
| A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+ |
| B.气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气 |
| C.灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,无K+ |
| D.将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2 |
用酸性氢氧燃料电池(乙池)为电源进行电解的实验装置(甲池,一定条件下可实现有机物的电化学储氢)如下图所示。甲池中A为含苯的物质的量分数为10%的混合气体,B为10mol混合气体其中苯的物质的量分数为24%,C为标准状况下2.8mol气体(忽略水蒸汽),下列说法不正确的是
| A.乙池中溶液的pH变大 |
| B.E处通入H2,C处有O2放出 |
| C.甲池中阴极区只有苯被还原 |
| D.导线中共传导11.2mol电子 |
下列说法正确的是
| A.煤经处理变为气体燃料的过程属于物理变化 |
| B.淀粉、油脂和蛋白质都是高分子化合物 |
| C.乙烯和乙醇均可使酸性KMnO4溶液褪色 |
| D.乙酸乙酯和植物油均可水解生成乙醇 |
下列实验中,依据实验操作及现象,得出的结论正确的是
| 操作 |
现象 |
结论 |
|
| A |
将水蒸气通过灼热的铁粉 |
粉末变红 |
铁与水在高温下发生反应 |
| B |
将充满NO2的密闭玻璃球浸泡在热水中 |
红棕色变深 |
反应2NO2(g) N2O4(g);ΔH<0 N2O4(g);ΔH<0 |
| C |
将少量的溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CCl4振荡 |
上层分别呈无色和紫红色 |
还原性:I->Br->Fe2+ |
| D |
向溶液X中加入稀盐酸,并将产生的无色气体通入澄清石灰水中 |
生成白色沉淀 |
溶液X中一定含有CO32-或SO32- |
下列叙述正确的是
| A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍,稀释后溶液的pH=4 |
| B.25℃时Ksp(AgCl)=1.8×10—10,向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度可能增大 |
| C.浓度均为0.1 mol·L-1的下列溶液,pH由大到小的排列顺序为:NaOH>Na2CO3>(NH4)2SO4>NaHSO4 |
| D.为确定H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH >7,则H2A是弱酸;若pH<7,则H2A是强酸 |
下列离子方程式书写正确的是
| A.H218O中投入Na2O2固体:2H218O+2Na2O2===4OH-+4Na++18O2↑ |
| B.Fe3O4与稀HNO3反应:Fe3O4+8H+===Fe2++2Fe3++4H2O |
C.向NaHCO3溶液中加入少量Ca(OH)2:HCO3-+Ca2++OH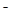 ===CaCO3↓+H2O ===CaCO3↓+H2O |
| D.将少量NaOH溶液加入到NH4HCO3溶液中:OH-+HCO3-===CO32-+H2O |