已知A、B、C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按如图进行反应。下列说法中不正确的是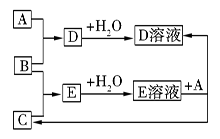
A.A、B、C中三种元素的任意两种元素形成的化合物所属物质类别可能是氧化物
B.A、B、C中三种元素形成的化合物所属物质类别一定不是碱
C.如果E溶液是一种强酸,则E溶液为盐酸
D.A、B、C中有一种金属且为A
下列反应的离子方程式正确的是
| A.过氧化钠固体与水反应制氧气:2O22—+2H2O=4OH-+O2↑ |
| B.在100ml浓度为1 mol · L-1的Fe(NO3)3的溶液中通入足量SO22Fe3++SO2+2H2O==2Fe2++SO42-+4H+ |
| C.1mo·L-1的NaAlO2溶液和2.5mol· L-1的盐酸等体积混合:2AlO2-+ 5 H+=Al(OH)3 ↓+ Al3++ H2 O |
| D.向碳酸钠溶液中逐滴加入与之等体积等物质的量浓度的稀醋酸:CO+H+=== HCO |
下图是部分短周期主族元素原子半径与原子序数的关系图。则下列说法正确的是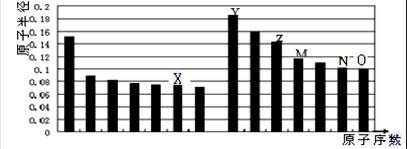
| A.Y、O两种元素的离子半径相比,前者较大 |
| B.Z的氧化物能分别溶解于Y的最高氧化物的水化物和O的氢化物的水溶液 |
| C.由X与Y两种元素组成的化合物只含离子键 |
| D.X、N两种元素的气态氢化物的稳定性相比,后者较强 |
下列说法正确的是
| A.蛋白质在空气中完全燃烧转化为水和二氧化碳 |
| B.汽油、甘油、花生油都属于酯类物质 |
| C.麦芽糖及其水解产物均能发生银镜反应 |
| D.燃煤产生的二氧化硫是引起雾霾的主要原因 |
由下列实验现象得出的结论正确的是
| 选项 |
实验现象 |
结论 |
| A |
取某Na2SO3溶液,加入足量的稀盐酸,产生气泡,再滴加BaCl2溶液,产生白色沉淀。 |
Na2SO3已部分被氧化 |
| B |
向2mL0.1mol/LNaOH溶液中滴加0.1mol/LMgCl2溶液3滴,出现白色沉淀后,再滴加3滴0.1mol/L FeCl3溶液,出现红褐色沉淀。 |
溶解度:Mg(OH)2>Fe(OH)3 |
| C |
向氯水中通入足量SO2,氯水褪色。 |
SO2具有漂白性 |
| D |
相同温度下,测等浓度的Na2CO3和Na2SO3水溶液的pH: pH (Na2CO3) > pH(Na2SO3)。 |
非金属性强弱:C>S |
钠-硫(Na/S8)电池是由固体电解质将两个液体电极隔开(如图),一个由钠-β-氧化铝固体电解质做成的中心管,将内室的熔融钠(熔点98℃)和外室的熔融硫(熔点119℃)隔开,并允许Na+ 通过。下列有关说法错误的是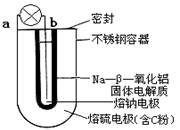
| A.放电时b为电池的负极 |
| B.充电时阴极反应式为:Na++e—=Na |
| C.充电时,阳极处发生还原反应 |
| D.放电时Na+ 可以穿过固体电解质流向a电极 |