是物质间发生化学反应时颜色的变化情况,下列选项中正确的是

| |
M |
N |
P |
Q |
| A |
NH3·H2O |
Ba(OH)2 |
铜 |
石蕊试液 |
| B |
Na |
BaCl2 |
FeO |
KSCN |
| C |
NaOH |
Ba(NO3)2 |
锌粉 |
KSCN |
| D |
NaHCO3 |
MgCl2 |
Fe |
石蕊试液 |
下列说法正确的是()
| A.明矾和漂白粉常用于水处理,两者的作用原理相同 |
| B.利用潮汐发电是将化学能转化为电能 |
| C.铝合金的大量使用是因为人们能用焦炭等还原剂从氧化铝中获取铝 |
| D.2009年12月中旬在哥本哈根召开的国际气候会议受到全球政要的广泛关注,减少工业生产大量排放二氧化碳等温室气体以抑制全球气候变暖成为该会议的主题 |
绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染,下列做法不符合绿色化学理念的是()
|
| A.研制水溶剂涂料替代有机溶剂涂料 |
B.用可降解塑料生产包装盒或快餐盒 |
| C.用反应:Cu +2H2SO4(浓)CuSO4+SO2↑+2H2O制备硫酸铜 | |
D.用反应: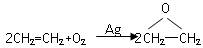 制备环氧乙烷 制备环氧乙烷 |
下列有关试剂的保存方法,错误的是()
| A.浓硝酸通常保存在棕色玻璃试剂瓶中 |
| B.过氧化钠盛放于塑料袋内,并保存在密闭的容器中 |
| C.氢氧化钠溶液保存在带橡皮塞的玻璃试剂瓶中 |
| D.新制的氯水保存在无色玻璃试剂瓶中 |
为证明溴丙烷中溴元素的存在,下列正确的操作步骤是()
①加入硝酸银溶液 ②加入氢氧化钠溶液
③加热 ④加入蒸溜水
⑤加稀硝酸至溶液呈酸性 ⑥加入氢氧化钠醇溶液
| A.②③⑤① | B.④③①⑤ | C.④⑥③① | D.⑥③⑤① |
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述正确的是()
| A.植物油不能使溴的四氯化碳溶液褪色 |
| B.淀粉水解的最终产物是葡萄糖 |
| C.葡萄糖能发生氧化反应和水解反应 |
| D.蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |