R、L、M三种主族元素,已知R+、L-具有相同电子层结构,M元素原子核电荷数比L元素原子核电荷数少9,L-在一定条件下可被氧化成LM3-,则下列说法正确的是
| A.R、L、M均属于短周期元素 |
| B.离子半径R+>L- |
| C.R、L、M三种元素组成的化合物中既含有离子键又含有共价键 |
| D.L的气态氢化物可形成氢键 |
a、b、c、d均为短周期元素,a的原子结构示意图为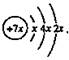 ,元素b的形成单质
,元素b的形成单质
|
可以与CO2发生置换反应,原子序数b<c<a,b与d形成的化合物电子式为
下列比较中正确的是
| A.原子半径c<d | B.呈得无素在同一周期 |
| C.气态氢化物的稳定性a<d | D.最高价氧化物对应的水化物的碱性b<c |
下列说法正确的是
①电解质溶液导电过程属于化学变化
②稀有气体不活泼的原因是它们原子的最外层都达到8电子稳定结构
③FeC12、CuS、NO都不能通过化合反应来制取
④SiO2是制造光导纤维的材料
| A.②④ | B.①④ | C.①③④ | D.②③ |
查阅资料发现,金属钠不仅能跟氧气和水反应,还能跟多种其它物质发生反应,其中包括与酒精在常温下反应。要研究金属钠跟酒精反应的性质以及它与水反应的异同 点,下列的研究方法中没有用到的是
| A.实验法 | B.观察法 | C.分类法 | D.比较法 |
已知:H2O(g)=H2O(l) △H1=-Q1 kJ/mol;
C2H5OH(g)=C2H5OH(l) △H2=-Q2 kJ/mol
C2H5OH(g)+3O2(g)=2CO2(g)+3 H2O(g) △H3=-Q3 kJ/mol
H2O(g) △H3=-Q3 kJ/mol
若使23g酒精液体完全燃烧,最后恢复到室温,则放出的热量是 多少kJ()
多少kJ()
| A.Q1+ Q2+Q3 | B.0.5(Q1+Q2+Q3) | C.0.5 Q2-0.5 Q3-1.5Q1 | D.1.5Q1-0.5Q2+0.5Q3 |
下列热化学方程式正确的是(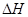 的绝对值均正确)
的绝对值均正确)
| A.C2H5OH(l)+3O2(g)= 2CO2(g)+3H2O(g);△H=—1367.0 kJ/mol(燃烧热) |
| B.NaOH(aq)+HCl(aq)= NaCl(aq)+H2O(l);△H=+57.3kJ/mol(中和热) |
| C.S(s)+O2(g)= SO2(g);△H=—269.8kJ/mol(反应热) |
| D.2NO2= O2+2NO;△H=+116.2kJ/mol(反应热) |