所谓合金,就是不同种金属(也包括一些非金属)在熔融状态下形成的一种熔合物。根据下列四种金属的熔、沸点,判断其中不能形成合金的是
| |
Na |
Cu |
Al |
Fe |
| 熔点/℃ |
97.5 |
1 083 |
660 |
1 535 |
| 沸点/℃ |
883 |
2 595 |
2 200 |
3 000 |
A.Cu和Al B.Fe和Cu C.Fe和Na D.Al和Na
利用下列可逆反应可以将粗镍转化为纯度99.9%的高纯镍: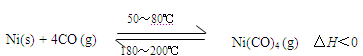
下列说法正确的是
| A.50~80℃时,适当增大压强,有利于Ni(CO)4的生成 |
| B.180~200℃时,气态的Ni(CO)4 会分解出纯Ni |
| C.提纯过程中,CO(g)的量不断减少 |
| D.温度越高,Ni(CO)4 (g)的转化率越低 |
下列离子方程式书写正确的是
| A.用稀硝酸洗涤做过银镜反应的试管:Ag + 4H+ + NO3¯ = Ag+ + NO↑ + 2H2O |
B.铝片跟氢氧化钠溶液反应:Al+2OH¯=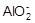 +H2↑ +H2↑ |
| C.碳酸钙溶于醋酸:CaCO3 + 2H+ = Ca2+ + CO2↑ + H2O |
D.苯酚钠溶液中通入少量CO2: -O¯+CO2+H2O = -O¯+CO2+H2O =  -OH +HCO3¯ -OH +HCO3¯ |
NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.在1 L 0.2 mol·L-1的Na2CO3溶液中含有CO32—的数目为0.2NA |
| B.0.1 mol Fe参加氧化还原反应,转移的电子数目一定是0.3NA |
| C.标准状况下22.4 L CH4和C2H4的混合气体所含氢原子数为4NA |
| D.理论上氢氧燃料电池正极消耗11.2 L标准状况下气体时,外线路通过电子数为NA |
某元素的原子3d能级上有1个电子,它的N能层上电子数是 ( )
| A.0 | B.2 | C.5 | D.8 |
下列说法正确的是 ( )
| A.原子核外电子排布式为1s2的原子与原子核外电子排布式为1s22s2的原子化学性质 相似 |
| B.Fe3+的最外层电子排布式为:3s23p63d5 |
C.基态铜原子的轨道表示式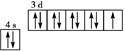 |
D.基态碳原子的轨道表示式 |