已知:Fe2O3(s) +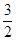 C(s)=
C(s)=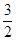 CO2(g) +2Fe(s) ΔH1="+234.1" kJ·mol-1,C(s)+ O2(g)=CO2(g) ΔΗ2="-393.5" kJ·mol-1,则2Fe(s) +
CO2(g) +2Fe(s) ΔH1="+234.1" kJ·mol-1,C(s)+ O2(g)=CO2(g) ΔΗ2="-393.5" kJ·mol-1,则2Fe(s) +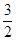 O2(g) =Fe2O3(s) 的ΔH是
O2(g) =Fe2O3(s) 的ΔH是
| A.-824.4 kJ·mol-1 |
| B.-627.6 kJ·mol-1 |
| C.-744.7 kJ·mol-1 |
| D.-169.4 kJ·mol-1 |
下列装置能构成原电池的是()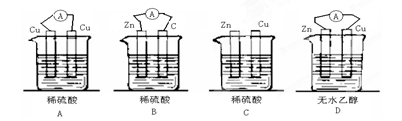
中小学生经常使用的涂改液中含有挥发性的有毒溶剂,应尽量不使用,以减少对身体的毒害及对环境的污染。该溶剂是()
| A.乙醇 | B.乙酸 | C.三氯乙烯 | D.甘油 |
曾对化学平衡进行研究并提出平衡移动原理的化学家是()
A 勒夏特列 B 门捷列夫 C 道尔顿 D 拉瓦锡
随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程上来,其主要的原因是()
| A.利用电池外壳的金属材料 | B.不使电池中渗泄的电解质溶液腐蚀其他物品 |
| C.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 | D.回收其中石墨电极 |
某温度、压强下,将一定量反应物通入密闭容器进行反应
SiCl4(g)+2H2(g) Si(s)+4HCl(g); ΔH=+QkJ/mol(Q>0),下列叙述正确的是 ( )
Si(s)+4HCl(g); ΔH=+QkJ/mol(Q>0),下列叙述正确的是 ( )
| A.反应过程中,若增大压强能提高SiCl4的转化率 |
| B.若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ |
| C.若单位时间内生成x molHCl的同时,生成x molH2,则反应达到平衡状态 |
| D.使用过量的H2或升高温度都可以提高SiCl4的转化率 |