下列各物质的学名是:Na2S2O3叫硫代硫酸钠;CaSx叫多硫化钙;Na2O2叫过氧化钠;KO2叫超氧化钾。试综合上述命名规律,分析回答:Na2CS3应读做
| A.硫代碳酸钠 | B.多硫碳酸钠 | C.过硫碳酸钠 | D.超硫碳酸钠 |
相同质量的钠在下列情况下产生氢气最多的是
| A.放在足量水中 |
| B.放在足量盐酸中 |
| C.放在足量CuSO4溶液中 |
| D.用刺有小孔的铝,包好放入足量水底中 |
实验用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体,经历下列过程,Fe3+在pH=5时已完全沉淀,其中分析不正确的是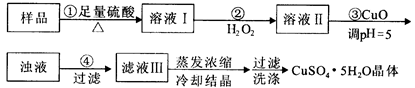
| A.利用CuCO3替代CuO也可调节溶液的pH,不影响实验结果 |
| B.步骤②中加入H2O2的目的是将Fe2+氧化成Fe3+ |
| C.上述冷却结晶若改用蒸发结晶也能得到上述产物 |
| D.配制240 mL 1mol·L-1的CuSO4溶液,需称量CuSO4•5H2O的质量为62.5g |
下列有关的计算分析不正确的是
| A.在反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O中,当有1 mol铜被氧化时,被还原的硝酸为2/3mol |
| B.将a mol硫化亚铁放入含3a mol H2SO4的浓硫酸中,充分反应后,氧化、还原产物分别是Fe3+、S和SO2,则放出的气体少于1.5a mol |
| C.室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不能支持燃烧。则a、b的关系为a=4b+3c |
| D.某溶液100 mL,其中含硫酸0.03 mol,硝酸0.04 mol,若在该溶液中投入1.92 g铜粉微热,反应后放出一氧化氮气体约为0.015 mol |
已知:还原性 >I-,氧化性
>I-,氧化性 ,在含0.3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是
,在含0.3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是
A.0~b间的反应可用如下离子方程式表示: |
| B.a点时消耗NaHSO3的物质的量为0.12mol |
| C.当溶液中的I-为0.4 mol时,加入的KIO3只能是0.4mol |
| D.b点时的还原产物可能是KI或NaI,b~c间的还原产物是I2 |