为探究足量锌与稀硫酸的反应速率(以v(H2)表示),向反应混合液中加入某些物质,下列判断正确的是
| A.加入NH4HSO4固体,v(H2)不变,生成H2量不变 |
| B.加入少量水,v(H2)减小,生成H2量减少 |
| C.加入CH3COONa固体,v(H2)减小,生成H2量不变 |
| D.滴加少量CuSO4溶液,v(H2)增大,生成H2量减少 |
两瓶均为棕黄色的氯化铁溶液和溴水,用下列试剂无法鉴别的是( )
| A.KSCN | B.CCl4 | C.NaOH | D.淀粉KI试纸 |
学生设计了如图的方法对A盐进行鉴定: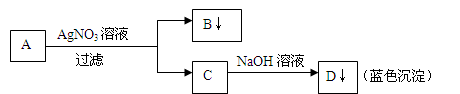
由此分析,下列结论中,正确的是( )
| A.A中一定有Fe3+ | B.C中一定有Cu2+ |
| C.B一定为AgBr沉淀 | D.A一定为CuCl2溶液 |
下列离子方程式书写正确的是( )
| A.氯气通入冷的氢氧化钠溶液中: Cl2 + 2OH-=Cl- + ClO- + H2O |
| B.铁粉与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C.氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| D.在氯化亚铁溶液中通入氯气:Cl2+Fe2+=Fe3++2Cl- |
在强酸性溶液中,能大量共存的离子组是( )
| A.NH4+、Na+、Cl-、SO42- | B.Cu2+、Ca2+、CO32-、Cl- |
| C.Al3+、 Ag+、NO3-、Cl- | D.K+、HCO3-、Cl-、 Na+ |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A.32g O2中含有的氧分子数为2NA |
| B.常温常压下,22.4L的SO2气体中含有的氧原子数为2NA |
| C.1.0 mol·L-1CH3COOH溶液中含有的H+数一定为NA |
| D.2.7g Al在与足量盐酸反应中失电子数为0.3NA |