浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随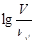 的变化如图所示,下列叙述错误的是
的变化如图所示,下列叙述错误的是
| A.MOH的碱性强于ROH的碱性 |
| B.ROH的电离程度:b点大于a点 |
| C.若两溶液无限稀释,则它们的c(OH-)相等 |
D.当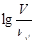 =2时,若两溶液同时升高温度,则 =2时,若两溶液同时升高温度,则  增大 增大 |
汽车尾气的无害化处理已成为当今汽车工业的一项重要课题,其基本原理是实现
2NO(g)+2CO(g) N2(g)+2CO2(g)的反应。关于该反应,下列说法正确的是
N2(g)+2CO2(g)的反应。关于该反应,下列说法正确的是
| A.只要使用合理的催化剂及载体,就可完全清除NO和CO |
| B.使用催化剂只能改变反应的速率不能改变反应的平衡常数 |
| C.假设该反应在密闭容器中进行,一段时间后达到平衡时c(NO)=c(CO) |
| D.恒容条件下,通入惰性气体可提高NO转化率 |
下物质分类组合正确的是
| A |
B |
C |
D |
|
| 强电解质 |
HCl |
酒精 |
CH3COOH |
NaCl |
| 弱电解质 |
NH3`H2O |
HClO |
BaSO4 |
NaOH |
下列叙述中,不能用平衡移动原理解释的是
| A.红棕色的NO2,加压后颜色先变深后变浅 |
| B.高压比常压有利于合成SO3的反应 |
| C.由H2(g)、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
| D.黄绿色的氯水光照后颜色变浅 |
下列事实中能说明醋酸是弱电解质的是
| A.用醋酸溶液作导电试验,灯光较暗 |
| B.醋酸(CH3COOH)是共价化合物 |
| C.醋酸不与氯化钠反应 |
| D.常温下1 mol・L-1醋酸溶液的c(H+)约为0.004 mol·L-1 |
下列反应中生成物总能量高于反应物总能量的是
| A.碳酸钙受热分解 | B.乙醇燃烧 |
| C.铝粉与氧化铁粉末反应 | D.氧化钙溶于水 |