室温下,向20.00 mL 1.000 mol·L-1氨水中滴入1.000 mol·L-1盐酸,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法正确的是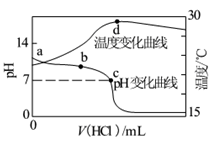
| A.氨水的电离程度a>b>c |
| B.a、d两点的溶液,水的离子积Kw(a)>Kw(d) |
| C.c点时消耗盐酸体积V(HCl)<20 .00ml |
| D.d点时溶液温度达到最高,之后温度略有下降,原因是NH3·H2O电离吸热 |
A的原子结构示意图为: ,其基态原子的价电子层电子排布式正确的是
,其基态原子的价电子层电子排布式正确的是
| A.3s23p2 | B.3d24s2 | C.4s24p2 | D.3s23p4 |
甲、乙两烧杯中各盛有100mL3mol/L的硫酸和氢氧化钠溶液,向两烧杯中分别加入A克的铝粉,反应结束后测得生成的气体体积为甲:乙=3:4,下列说法正确的是
| A.参加反应的H2SO4为0.2mol | B.参加反应的NaOH约为0.27mol |
| C.加入铝粉的质量A=5.4 | D.与硫酸反应的铝粉的质量7.2g |
三氟化氮(NF3)(提示氟只有两种价态:-1,0)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O=2NO+HNO3+9HF。下列有关该反应的说法正确的是
| A.NF3是氧化剂,H2O是还原剂 |
| B.还原剂与氧化剂的物质的量之比为2:1 |
| C.若生成0.2molHNO3,则转移0.2mol电子 |
| D.若1molNF3被氧化反应转移电子数为2NA |
下列各组物质相互作用时,生成物不随反应条件或反应物的量变化而变化的是
| A.Na和O2 | B.NaOH和CO2 | C.NaHCO3和NaOH | D.C和O2 |
某溶液中含有Cl-和I-的物质的量浓度相同。为了氧化I-而不使Cl-氧化,试根据下列三个反应判断,可选用的氧化剂是:①2Fe3++2I-=2Fe2++I2②2Fe2++Cl2=2Fe3++2Cl-③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O
| A.FeCl2 | B.KMnO4 | C.浓盐酸 | D.FeCl3 |