下列指定反应的离子方程式正确的是
| A.Fe和稀硝酸反应 Fe+2H+===Fe2++H2↑ |
| B.将Fe(NO3)3溶液与少量HI混合:8H++2NO3-+6I-===4H2O+3I2+2NO↑ |
| C.用过量氨水吸收SO2的反应:NH3·H2O+SO2===NH4++HSO3- |
| D.少量Ca(OH)2和NaHCO3反应 Ca2++OH-+HCO3-===CaCO3↓+H2O |
下列说法正确的是()
| A.直径为20nm的纳米碳酸钙属于胶体 |
| B.海水中提取镁的各步均为氧化还原反应 |
| C.可溶性铁盐和铝盐可用作净水剂 |
| D.光导纤维是一种新型硅酸盐材料 |
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断不正确的是()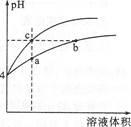
| A.a、b、c三点溶液的Kw相同 |
| B.b点溶液中c(H+)+c(NH3·H2O)=c(OH-) |
| C.用等浓度的NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液的体积Vb>Vc |
| D.a、b、c三点溶液中水的电离程度a>b>c |
NA表示阿伏加德罗常数,下列说法正确的是()
| A.在0.1molNaHSO4晶体中阳离子与阴离子总数为0.3NA |
| B.1.0L0.1mol·L-1NH4NO3溶液中含有的铵根离子数是0.1×6.02×1023 |
| C.7.8gNa2O2与足量CO2反应,转移的电子数为0.1NA |
| D.向仅含0.2molFeI2的溶液中持续通入氯气,当有0.1molFe2+被氧化时,需通入标况下C121.12L |
X、Y、Z、W四种物质的转化关系.下列组合中不符合该关系的是()
| A |
B |
C |
D |
|
| X |
HCl |
Na2CO3 |
Na2O2 |
SO2 |
| Y |
FeCl2 |
CO2 |
NaOH |
Na2SO3 |
| Z |
Cl2 |
CaCO3 |
Na2CO3 |
H2SO4 |
| W |
FeCl3 |
Ca(HCO3)2 |
NaHCO3 |
NaHSO3 |

A.A B.BC.CD.D
将几种铁的氧化物的混合物加入100mL、7mol•L―1的盐酸中。氧化物恰好完全溶解,在所得的溶液中通入0.56L(标况)氯气时,恰好使溶液中的Fe2+完全转化为Fe3+,则该混合物中铁元素的质量分数为()
| A.72.4% | B.71.4% | C.79.0% | D.63.6% |