NA表示阿伏加德罗常数,下列叙述正确的是
| A.0.1mol•L﹣1的Na2CO3溶液中含CO32﹣为0.1NA |
| B.3.2 g O2和O3的混合气中氧原子数为0.2NA |
| C.1mol H3O+含质子数为10 NA |
| D.标准状况下,22.4 L乙醇的分子数为NA |
NM-3和D-58是正处于临床试验阶段的小分子抗癌药物,结构如下:
关于NM-3和D-58的叙述,错误的是
| A.都能与NaOH溶液反应,原因不完全相同 |
| B.都能与溴水反应,原因不完全相同 |
| C.都不能发生消去反应,原因相同 |
| D.遇FeCl3溶液都显色,原因相同 |
下列各组转化,属于同一有机反应类型的是
| A.由溴乙烷制乙烯;由乙炔制乙烯 |
| B.乙醛转化为乙酸;乙醛转化为乙醇 |
| C.乙烯使溴水褪色;甲苯使酸性KMnO4溶液褪色 |
| D.由硝酸与苯反应制硝基苯;由硝酸与甘油反应制硝化甘油 |
下列说法正确的是
| A.“辛烷值”可用来表示汽油的质量,异辛烷的爆震程度最小。图1是异辛烷的球棍模型,系统命名为2,4,4三甲基戊烷 |
| B.用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液 |
| C.乙酸乙酯中除去乙酸:用饱和碳酸钠溶液洗涤后分液 |
| D.图2化合物核磁共振氢谱图中有5个吸收峰 |
仅用一种试剂即可区分酒精、苯酚溶液、己烯、甲苯等四种无色液体,这种试剂可以是:
| A.FeCl3溶液 | B.溴水 | C.高锰酸钾溶液 | D.金属钠 |
1丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为 115℃ ~125℃,反应装置如图.下列对该实验的描述错误的是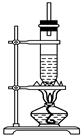
| A.不能用水浴加热 |
| B.长玻璃管起冷凝回流作用 |
| C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤 |
| D.加入过量乙酸可以提高1丁醇的转化率 |