关于某无色溶液中所含离子的鉴别,下列判断正确的是
| A.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl-存在 |
| B.通入Cl2后,溶液变为黄色,加入淀粉溶液后溶液变蓝,可确定有I-存在 |
| C.加入Ba(NO3)2,生成白色沉淀,加稀盐酸沉淀不消失,可确定有SO42-存在 |
| D.加入盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO32-存在 |
用高铁酸钠(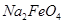 )对河湖水消毒是城市饮水处理的新技术。已知反应
)对河湖水消毒是城市饮水处理的新技术。已知反应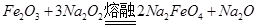 ,下列说法正确的是
,下列说法正确的是
| A.Na2O2既是氧化剂又是还原剂 |
| B.3 mol Na2O2发生反应,有12 mol电子转移 |
C.在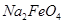 中Fe为+4价,具有强氧化性,能消毒杀菌 中Fe为+4价,具有强氧化性,能消毒杀菌 |
D.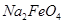 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
下列关于有机物的叙述不正确的是
| A.甲烷、甲苯、乙醇、乙酸都可以发生取代反应 |
| B.煤中含有苯、甲苯、二甲苯等芳香烃,可通过干馏制取 |
| C.乙酸乙酯在无机酸或碱存在时都能发生水解反应 |
| D.淀粉、纤维素、蛋白质都属于高分子化合物 |
下列溶液中,微粒浓度关系正确的是
A.含有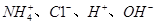 的溶液中,其离子浓度一定是: 的溶液中,其离子浓度一定是: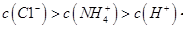 >c(OH-) >c(OH-) |
B.pH=6的醋酸与醋酸钠的混合溶液中,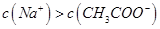 |
C.0.1 mol/L的Na2S溶液中,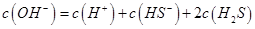 |
D.pH=3的一元酸和pH=11的一元碱等体积混和后的溶液中,一定是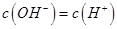 |
下列有关实验原理或实验操作正确的是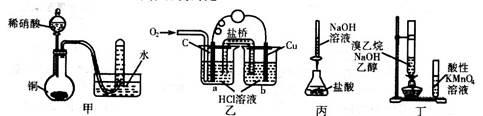
| A.用甲装置验证铜与稀硝酸的反应产物是NO |
B.通过乙装置实现化学反应: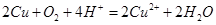 |
| C.用丙装置测定盐酸的浓度 |
| D.用丁装置检验溴乙烷与NaOH醇溶液共热有乙烯生成 |
铁的氧化物可用于脱除煤气中的H2S,有关反应原理如下:
①Fe3O4(s)+3H2S(g)+H2(g)⇌3FeS(s)+4H2O(g)
②Fe2O3(s)+2H2S(g)+H2(g)⇌2FeS(s)+3H2O(g)
③FeO(s)+H2S(g)⇌FeS(s)+H2O(g)
温度与上述各反应的平衡常数的关系如图所示。下列有关说法正确的是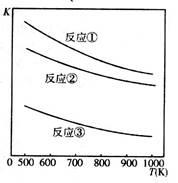
| A.反应①、②、③中铁的氧化物都是氧化剂 |
| B.反应①、②、③的正反应都是放热反应 |
| C.反应①、②、③中,温度越高H2S的的脱除率越高 |
| D.反应①、②、③中,压强越大H2S脱除率越高 |