下列说法正确的是
| A.浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
| B.用可见光束照射以区别溶液和胶体 |
| C.稀豆浆、硅酸、氯化铁溶液均为胶体 |
| D.H+、K+、S2-、Br-能在Fe(OH)3胶体中大量共存 |
下列物质中含有非极性键的分子是( )
| A.MgF2 | B.N2 | C.CO2 | D.Na2O2 |
25℃、101 kPa下,CO、HCOOH、CH4和CH3OH的燃烧热依次是67.6 kJ/mol、62.8kJ/mol、890.3 kJ/mol、726kJ/mol,则下列热化学方程式不正确的是()
| A.CO(g)+O2(g)=CO2(g);DH=-67.6 kJ/mol |
| B.HCOOH(1)+O2(g)=CO2(g)+H2O(1);DH=-62.8 kJ/mol |
| C.CH4g)+2O2(g)=CO2(g)+2H2O(g);DH=-890.3 kJ/mol |
| D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l);DH=-1452 kJ/mol |
可逆反应aA(g)+bB(s) cC(g)+dD(g)在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是()
cC(g)+dD(g)在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是()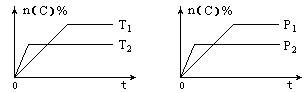
| A.温度降低,化学平衡向逆反应方向移动 |
| B.使用催化剂,C的物质的量分数增加 |
| C.化学方程式系数a<c+d |
| D.无法根据图像确定改变温度后化学平衡移动方向 |
下列变化一定属于化学变化的是()
①导电②爆炸③缓慢氧化④品红褪色⑤无水硫酸铜自白变蓝⑥工业制O2⑦白磷转化为红磷⑧久置浓硝酸变黄
| A.②③④⑦⑧ | B.③④⑤⑦⑧ | C.②③⑥⑦ | D.④⑤⑦⑧ |
某实验室仅有如下仪器或用具:烧杯、铁架台、铁圈、三脚架、漏斗、分液漏斗、石棉网、酒精灯、玻璃棒、量筒、蒸发皿、圆底烧瓶、火柴。从缺乏仪器的角度看,不能进行的实验项目是 ( )
| A.蒸发 | B.萃取 | C.液体过滤 | D.升华 |