黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)==K2S(s)+N2(g)+3CO2(g) ΔH=" x" kJ·mol-1
已知碳的燃烧热ΔH1=" a" kJ·mol-1 S(s)+2K(s)==K2S(s) ΔH2=" b" kJ·mol-1
2K(s)+N2(g)+3O2(g)==2KNO3(s) ΔH3=" c" kJ·mol-1 则x为
| A.3a+b-c | B.c-3a-b | C.a+b-c | D.c-a-b |
下列过程需要吸收热量的是()
①水蒸气冷凝②煅烧石灰石③浓硫酸稀释④酸碱发生中和反应⑤生石灰跟水反应生成熟石灰⑥干冰升华⑦液氨汽化⑧水分解为氢气和氧气⑨氢原子两两结合为氢分子
| A.①②⑤⑥⑨ | B.②③⑥⑨ | C.①④⑤⑦⑧ | D.②⑥⑦⑧ |
根据下面信息,判断下列叙述中正确的是 ()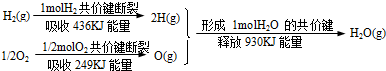
| A.1molH2和0.5molO2所具有的总能量低于1mol气态H2O所具有的总能量 |
| B.氢气跟氧气反应生成水的同时吸收能量 |
| C.1molH2跟1/2molO2反应生成1molH2O(l)释放能量一定是245kJ |
| D.2molH2(g)跟1molO2(g)反应生成2molH2O(g)释放能量490kJ |
在短周期元素中,A元素的最高正化合价和最低负化合价的绝对值之差为6,A元素与B元素可以形成化合物BA2,A的阴离子与B的阳离子具有相同的电子层结构,则该化合物是()
| A.MgCl2 | B.CaCl2 | C.SiO2 | D.CS2 |
已知钋的原子序数是84,是一种放射性元素,被称为世界上最毒的物质。钋在元素周期表中的位置是
| A.第七周期第ⅥA族 | B.第六周期第ⅥA族 |
| C.第六周期第ⅡA族 | D.第五周期第ⅥA族 |
已知锂和镁在元素周期表中有特殊“对角线”关系,它们的性质非常相似。下列有关锂及其化合物叙述正确的是()
| A.Li2SO4难溶于水 | B.Li与N2反应产物是Li3N |
| C.LiOH易溶于水 | D.LiOH与Li2CO3受热都很难分解 |