25℃时,在10mL浓度均为0.1mol/L的NaOH和NH3•H2O混合溶液中滴加0.1mol•L﹣1盐酸,下列有关溶液中粒子浓度关系正确的是
| A.未加盐酸时:c(OH﹣)>c(Na+)=c(NH3•H2O) |
| B.加入10mL盐酸时:c(NH4+)+c(H+)=c(OH﹣) |
| C.加入盐酸至溶液pH=7时:c(Cl﹣)=c(Na+) |
| D.加入20mL盐酸时:c(Cl﹣)=c(NH4+)+c(Na+) |
分子式为C5H12O的醇与和它相对分子质量相等的一元羧酸进行酯化反应,生成的酯共有(不考虑立体异构)()
| A.15种 | B.16种 | C.17种 | D.18种 |
某工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等)。下列对该产品的描述不正确的是() 
A. 官能团为碳碳双键、羧基
B. 与CH2=CHCOOCH3互为同分异构体
C. 能发生氧化反应
D. 分子中所有原子可能在同一平面
乙二酸可以被强氧化剂氧化为CO2,现有0.10mol/L乙二酸溶液20mL,恰好被4×10-3molVO2+ 所氧化,则此反应的还原产物VOn+中n的值为()
| A.5 | B.4 | C.3 | D.2 |
铁溶于一定浓度的硝酸时,发生反应的离子方程式为:
aFe+bNO3-+cH+═dFe2++fFe3++gNO↑+hNO2↑+kH20,下列有关推断中,不正确的是( )
| A.2d+3f=3g+h |
| B.c+b=2d+3f |
| C.HNO3的氧化性强于Fe3+ |
| D.反应中每消耗5.6gFe,转移0.2mol~0.3mole- |
下列实验可达到实验目的的是( )
①将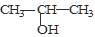 与NaOH的醇溶液共热制备CH3—CH═CH2
与NaOH的醇溶液共热制备CH3—CH═CH2
②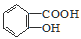 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备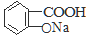
③向CH3CH2Br中滴入AgNO3溶液以检验溴元素
④用溴水即可检验CH2=CH-CHO中的碳碳双键
| A.只有① | B.只有①④ | C.只有①③④ | D.都不能 |