NA表示阿伏加德罗常数,下列说法中正确的是
①等物质的量的N2和CO所含分子数均为NA
②常温下,4 g CH4含有NA个C-H共价键
③1 mol Na2O2与水完全反应时转移电子数为2NA
④将NA个NH3分子溶于1 L水中得到1 mol·L-1的氨水
⑤25 ℃时,pH=12的1.0 L NaClO溶液中水电离出的OH-的数目为0.01NA
⑥1 mol SO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子
| A.①③⑤ | B.②⑤ | C.②④⑥ | D.②③⑤ |
用已准确称量过的氯化钠固体配制2.00mol·L-1的NaCl溶液0.2L,需要用到的仪器是:
①坩埚②分液漏斗③容量瓶④烧杯⑤胶头滴管⑥烧瓶⑦玻璃棒⑧托盘天平⑨药匙
| A.③④⑤⑦⑨ | B.①②⑤⑥⑧ | C.③④⑤⑦ | D.③④⑤⑥ |
下列物质所发生的化学反应中,由于反应物的用量不同而得到不同产物的是
①铁与稀硝酸②AgNO3溶液与氨水溶液③碳酸钠溶液与稀盐酸④铁与氯气⑤NaAlO2溶液和稀盐酸⑥FeCl3溶液与Na2S溶液
| A.全部都是 | B.①②③⑤⑥ | C.①②③⑤ | D.③④⑤ |
某同学通过系列实验探究Mg及其化合物的性质, 操作正确且能达到目的的是
操作正确且能达到目的的是
| A.将NaOH溶液缓慢滴入MgSO4溶液中,观察Mg(OH)2沉淀的生成 |
| B.将水加入浓硫酸中得到稀硫酸,置镁片于其中探究讨Mg的活泼性 |
| C.将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
| D.将Mg(OH)2沉淀转入表面皿中,加足量稀盐酸,加热蒸干得无水MgCl2固体 |
下列实验方案中,不能测定Na2CO3和NaHCO3,混合物中Na2CO3质量分数的是
| A.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| C.取a克混合物充分加热,得b克固体 |
| D.取a克混合物与足量Ca(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
下列说法中正确的是
| A.浓硫酸滴在润湿的蓝色石蕊试纸上,试纸先变红,然后褪色,最后变黑,说明浓硫酸具有酸性、氧化性和吸水性 |
B.样品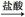 无明显现象 无明显现象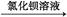 出现白色沉淀,说明样品中含SO42- 出现白色沉淀,说明样品中含SO42- |
| C.常温下浓硫酸能用铁制容器盛装,说明浓硫酸与Fe不反应 |
| D.样品中加入盐酸得到使澄清石灰水变浑浊的气体,说明样品中含CO32-或HCO3- |