将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如右图所示。下列说法正确的是
| A.苛性钾溶液中KOH的物质的量是0.09mol |
| B.ClO3-的生成是由于氯气的量的多少引起的 |
| C.在酸性条件下ClO-和ClO3-可生成Cl2 |
| D.反应中转移电子的物质的量是0.21mol |
乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是
①分子式为C12H20O2
②能使酸性KMnO4溶液褪色
③能发生加成反应,但不能发生取代反应
④它的同分异构体中可能有芳香族化合物,
且属于芳香族化合物的同分异构体有8种
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol
| A.①②③ | B.①②⑤ | C.①②⑤⑥ | D.①②④⑤ |
下列说法正确的是
| A.酸和醇反应一定能生成酯,且酯化反应是可逆反应 |
B.实验证实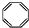 可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 |
C.DDT的结构简式为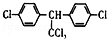 ,分子中最多有14个碳原子共平面 ,分子中最多有14个碳原子共平面 |
D.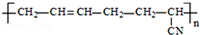 的单体是CH3﹣C≡C﹣CH3和CH2=CH﹣CN 的单体是CH3﹣C≡C﹣CH3和CH2=CH﹣CN |
下列说法错误的是
| A.鸡蛋清和淀粉可以用浓硝酸鉴别 |
| B.用甘氨酸和丙氨酸缩合最多可形成4种二肽 |
| C.分子式为C5H8O2,既与碳酸钠溶液反应又与溴的四氯化碳溶液反应的有机物有8种 |
D.乳酸薄荷醇酯(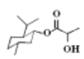 )仅能发生水解、氧化、消去反应 )仅能发生水解、氧化、消去反应 |
下列有关化学反应表达正确的是
A.服用阿司匹林过量出现水杨酸( )中毒反应,可静脉注射NaHCO3溶液: )中毒反应,可静脉注射NaHCO3溶液: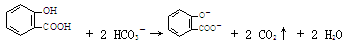 |
B.甲醛溶液与足量的银氨溶液共热:HCHO+4[Ag(NH3)2]++4OH- CO32- +2NH4++4Ag↓+6NH3+2H2O CO32- +2NH4++4Ag↓+6NH3+2H2O |
C.向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH- CH2BrCOO-+H2O CH2BrCOO-+H2O |
| D.苯酚钠溶液中通入少量CO2: CO2+H2O+2C6H5O- → 2C6H5OH+2CO32- |
下列叙述及评价均合理的是
| 选项 |
叙述 |
评价 |
| A |
乙酸乙酯在H218O中水解,产物乙醇中将含有18O |
错,根据酯的水解规律,产物乙酸中将含有18O同位素,而乙醇则没有。 |
| B |
淀粉与20%的硫酸混合溶液在沸水浴中充分加热后滴加碘水无蓝色现象,则说明淀粉水解完全 |
错,淀粉水解后未加碱中和至溶液呈碱性。 |
| C |
向卤代烃水解后的溶液中加入AgNO3溶液,根据沉淀颜色可以判断卤素原子种类 |
对,水解后溶液中有卤化氢,与AgNO3溶液反应生成卤化银沉淀。 |
| D |
可以用新制的Cu(OH)2悬浊液鉴别乙醇溶液、乙酸溶液和葡萄糖溶液 |
错,用新制的Cu(OH)2悬浊液不能鉴别乙醇溶液和乙酸溶液。 |