下列有关物质的性质与应用相对应的是
| A.二氧化锰具有强氧化性,可用作H2O2分解的氧化剂 |
| B.浓硝酸在常温下能使铝钝化,可用铝槽车运输浓硝酸 |
| C.K2FeO4具有还原性,可用于自来水的杀菌消毒 |
| D.SO2具有漂白性,能使紫色KMnO4溶液褪色 |
硫代硫酸钠溶液与稀硫酸反应的化学方程式为Na2S2O3+H2SO4===Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
对于反应A(g)+3B(g) 2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
A.v(A)=0.02 mol/(L·s) B.v(B)=0.03 mol/(L·s)
C.v(B)=0.90 mol/(L·min) D.v(C)=0.60 mol/(L·min)
对于反应:CaCO3+2HCl=CaCl2+H2O+CO2↑,下列说法正确的是
| A.用HCl和CaCl2表示的反应速率数据不同,但所表示的意义相同 |
| B.不能用CaCO3的浓度变化来表示反应速率,但可用水来表示 |
| C.用H2O和CO2表示的化学反应速率相同 |
| D.用CaCl2浓度的减小表示其反应速率 |
已知:(1)Zn(s)+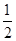 O2(g)===ZnO(s)ΔH=-348.3 kJ·mol-1
O2(g)===ZnO(s)ΔH=-348.3 kJ·mol-1
(2)2Ag(s)+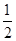 O2(g)===Ag2O(s)ΔH=-31.0 kJ·mol-1
O2(g)===Ag2O(s)ΔH=-31.0 kJ·mol-1
则Zn(s)+Ag2O(s)===ZnO(s)+2Ag(s)的ΔH等于
| A.-317.3 kJ·mol-1 | B.-379.3 kJ·mol-1 |
| C.-332.8 kJ·mol-1 | D.317.3 kJ·mol-1 |
下列热化学方程式书写正确的是(ΔH的绝对值均正确)
| A.C2H5OH(l)+3O2(g)==2CO2(g)+3H2O(g)ΔH=-1367.0 kJ/mol(燃烧热) |
| B.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l) ΔH=+57.3 kJ/mol(中和热) |
| C.S(s)+O2(g)==2SO2(g) ΔH=-296.8 kJ/mol(反应热) |
| D.2NO2==O2+2NOΔH=+116.2 kJ/mol(反应热) |