在乙烯分子中有5个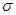 键、一个
键、一个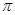 键,它们分别是
键,它们分别是
| A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键 |
| B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键 |
| C.C-H之间是sp2形成的σ键,C-C之间是未参加杂化的2p轨道形成的π键 |
| D.C-C之间是sp2形成的σ键,C-H之间是未参加杂化的2p轨道形成的π键 |
室温下,下列关于pH均为9、体积均为10mL的NaOH溶液和CH3COONa溶液比较的说法,正确的是()
| A.两种溶液中的c(Na+)相等 |
| B.分别加热到相同温度时,CH3COONa溶液的pH小 |
| C.分别加水稀释到100mL时,两种溶液的pH依然相等 |
| D.两溶液中由水电离出的c(OH-)之比为10-9/10-5 |
下列不属于配合物的是
| A.[Cu(H2O)4]SO4·H2O | B.[Ag(NH3)2]OH |
| C.KAl(SO4)2·12H2O | D.Na[AlF6] |
下列分子中的中心原子杂化轨道的类型相同的是
| A.CO2SO2 | B.C2H4C2H2 | C.BeCl2 BF3 | D.NH3 CH4 |
三氯化磷分子的空间构型是三角锥形而不是平面正三角形,下列关于三氯化磷分子空间构型理由的叙述,不正确的是
| A.PCl3分子中三个共价键的键长,键角都相等 |
B.PCl3分子中的P-Cl键 属于极性共价键 属于极性共价键 |
| C.PCl3分子中三个共价键键能,键角均相等 |
D.P Cl3是非极性分子 Cl3是非极性分子 |
下列各组分子中,都属于含极性键的非极性分子的是
| A.CO2H2S | B.C2H4CH4 | C.C60 C2H4 | D.NH3 HCl |