汽车剧烈碰撞时,安全气囊中发生反应: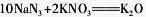
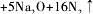 ,则下列说法正确的是
,则下列说法正确的是
| A.KNO3是还原剂,其中N元素被氧化 |
B.生成物中的N2是氧化产物,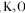 是还原产物 是还原产物 |
| C.若有65 g NaN3参加反应,则被氧化N的物质的量为3.2mol |
| D.每转移1 mol e一,可生成标准状况下N2的体积为35.84L |
高炉炼铁过程中发生的反应:1/3Fe2O3(s)+CO(g) 2/3Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表,下列说法不正确的是
2/3Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表,下列说法不正确的是
| 温度/℃ |
1000 |
1150 |
1300 |
| 平衡常数 |
4.0 |
3.7 |
3.5 |
A.△H<0
B.该反应的平衡常数表达式是
C.其他条件不变,向平衡体系充入CO2气体,K值减小
D.其他条件不变,升高温度,可以降低CO的平衡转化率
100 mL 6 mol·L-1 H2SO4与过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成H2的总量,可向反应物中加入适量
| A.醋酸钠溶液 | B.NaCl固体 | C.硫酸铜溶液 | D.硝酸钠溶液 |
下列叙述正确的是
| A.焓变是一个与反应能否自发进行有关的因素,多数能自发进行的反应都是放热反应 |
| B.增大压强是通过提高活化分子的百分数来提高反应速率 |
| C.氮的固定只有在高温、高压、催化剂的条件下才能实现 |
| D.水煤气是可再生能源 |
下列实验操作正确的是
| A.用上图装置测定中和热 |
| B.中和滴定过程中,眼睛应注视锥形瓶内溶液颜色的变化 |
C.研究H+浓度对该平衡:Cr2O72- + H2O 2CrO42- +2H+的影响,往5mL 0.1mol/L K2CrO4溶液加入5mL 0.1mol/L的稀硫酸 2CrO42- +2H+的影响,往5mL 0.1mol/L K2CrO4溶液加入5mL 0.1mol/L的稀硫酸 |
| D.测定溶液的pH值时,用玻璃棒蘸取少量溶液点在湿润的pH试纸上再与标准比色卡对照 |
下物质分类组合正确的是
| A |
B |
C |
D |
|
| 强电解质 |
AlCl3 |
HClO4 |
H3PO4 |
HClO |
| 弱电解质 |
CH3COOH |
HF |
BaSO4 |
Ca(OH)2 |
| 非电解质 |
酒精溶液 |
NH3 |
H2O |
SO2 |