下列说法中不正确的是
A.在燃煤中加入石灰石可减少SO2排放,发生的反应为2CaCO3 +2SO2 +O2 2CO2 +2CaSO4 2CO2 +2CaSO4 |
| B.C02通入水玻璃可以得到硅酸沉淀 |
| C.硅主要以单质、氧化物、硅酸盐的形式存在于自然界中 |
| D.氢氟酸能够雕刻玻璃,故不能用玻璃瓶来盛装氢氟酸 |
已知:A(g)+ 3B(g) M(g)+ N(g); ΔH=-49.0 kJ•mol-1。一定条件下,向体积为2 L的密闭容器中充入2 mol A和6molB,测得A和M的浓度随时间变化曲线如图所示。下列叙述中,正确的是
M(g)+ N(g); ΔH=-49.0 kJ•mol-1。一定条件下,向体积为2 L的密闭容器中充入2 mol A和6molB,测得A和M的浓度随时间变化曲线如图所示。下列叙述中,正确的是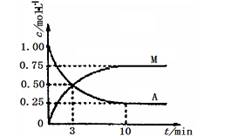
A、充分反应后该反应放出98 kJ的热量
B、10min后,升高温度能使n(M)/n(A)增大
C、3min时B的生成速率是M生成速率的3倍
D、反应到达平衡时刻B的转化率为75%
将0.4gNaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是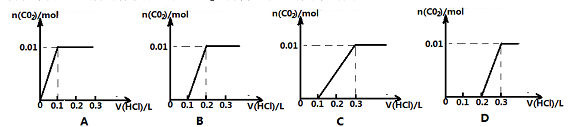
下列叙述正确的是
| A.0.1mol /L CH3COONa溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B.Na2CO3溶液加水稀释后,恢复至原温度,pH增大和KW不变 |
| C.一定温度下,pH=6的HCl溶液和pH=6的NH4Cl溶液中,c(H+)相等 |
| D.在Na2S溶液中加入AgCl固体,溶液中c(S2-)不变化 |
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)的关系如下图所示。反应中镁和铝的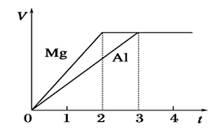
| A.摩尔质量之比为2∶3 |
| B.失去的电子数之比为8∶9 |
| C.反应速率之比为2:3 |
| D.质量之比为4∶3 |
过氧化钠可作为氧气的来源。常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了14g,反应中有关物质物理量正确的是(NA表示阿伏加德罗常数)