向50 mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10 mL,将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0.1 mol/L的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是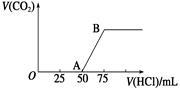
| A.OA段所发生反应的离子方程式: H++OH-==H2O;CO32- +H+ ==HCO |
| B.NaOH在吸收CO2后,所得溶液的溶质为NaOH和Na2CO3,其物质的量浓度之比为1∶1 |
| C.产生的CO2体积(标准状况下)为0.056 L |
| D.原NaOH溶液的物质的量浓度为0.5 mol·L-1 |
下列物质全部属于纯净物的是
| A.福尔马林、白酒、食醋 | B.甘油、氯仿、乙醇钠 |
| C.苯、汽油、无水乙醇 | D.二氯乙烷、聚氯乙烯、苯酚 |
在托盘天平的两盘中各放入一个质量相等的烧杯,两烧杯中各盛有100mL1mol/L 硫酸溶液,向两烧杯中分别加入各组中的两种物质,反应后天平保持平衡的是
| A.0.1mol Zn,0.1mol Fe | B.1mol Fe,1mol Zn |
| C.1g Zn,1g Fe | D.10g Zn,10g Fe |
两个不同容积的容器中分别盛有H2、O2,已知两个容器中气体的温度、密度都相等,下列说法一定正确的是
| A.两种气体质量相等 |
| B.两种气体的物质的量之比为16︰1 |
| C.两种气体压强比为16︰1 |
| D.两种气体体积比为1︰16 |
下图的实验装置用来分离CO2和CO 气体并干燥。图中a 为止水夹,b 为分液漏斗的活塞,通过Y 型管和止水夹分别接c.d 两球胆,现装置内的空气已排尽。为使实验成功,甲、乙、丙分别盛放的溶液是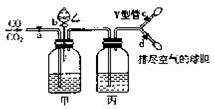
| A.饱和NaHCO3溶液、12mol·L-1盐酸、18.4mol·L-1H2SO4 |
| B.饱和Na2CO3溶液、2mol·L-1 H2SO4.、饱和NaOH 溶液 |
| C.饱和NaOH 溶液、2mol·L-1 H2SO4、18.4mol·L-1H2SO4 |
| D.18.4mol·L-1H2SO4、饱和NaOH 溶液、18.4mol·L-1H2SO4 |
下列溶液与30mL 1 mol·L-1 NaNO3溶液中NO3-物质的量浓度相等的是
| A.10 mL 1 mol·L-1 NaNO3溶液 |
| B.10 mL 1 mol·L-1 Al(NO3)3溶液 |
| C.15 mL 2 mol·L-1 AgNO3溶液 |
| D.10 mL 1.5 mol·L-1 Cu(NO3)2溶液 |