下列说法正确的是
| A.实验中需用0.20 mol·L-1的NaOH溶液950mL,配制时应称取NaOH的质量8.0g |
| B.升高NH4Cl溶液温度,其水的离子积常数和pH均增大 |
| C.水比硫化氢稳定的原因是水分子间存在氢键 |
| D.在pH等于2的醋酸溶液中加入少量0.01 mol·L-1的稀盐酸,溶液的pH会变小 |
在反应C(s)+CO2(g)=2CO(g)中,能使反应速率加快的是
①增大压强②升高温度③将C粉碎④通CO2气体⑤加入足量木炭粉
| A.①②③④ | B.①②③ | C.①②④ | D.全部 |
甲:在试管中加入1 g粉末状大理石,加入4 mol/L盐酸20 mL(过量);
乙:在试管中加入2 g颗粒状大理石,加入4 mol/L盐酸20 mL(过量);
生成体积(折算成标准状况)V(CO2)同反应时间t的关系曲线图合理的是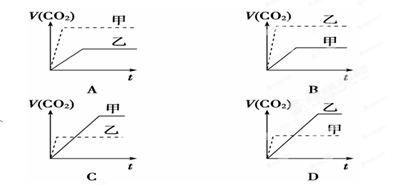
实验室测得4 mol SO2发生下列化学反应:2SO2(g)+O2(g) 2SO3(g)ΔH=-196 kJ/mol。当放出313.6 kJ热量时,SO2转化率最接近于
2SO3(g)ΔH=-196 kJ/mol。当放出313.6 kJ热量时,SO2转化率最接近于
| A.40% | B.50% | C.80% | D.90% |
反应N2+3H2 2NH3 ,开始时N2的浓度为3 mol·L-1,H2的浓度为5 mol·L-1,3 min后测得NH3浓度为0.6 mol·L-1,则此时间内,下列反应速率表示正确的是
2NH3 ,开始时N2的浓度为3 mol·L-1,H2的浓度为5 mol·L-1,3 min后测得NH3浓度为0.6 mol·L-1,则此时间内,下列反应速率表示正确的是
| A.v(H2)=0.3 mol·L-1·min-1 | B.v(NH3)=0.2 mol·L-1·s-1 |
| C.v(N2)=1.0mol·L-1·min-1 | D.v(H2)=1.67 mol·L-1·min-1 |
白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ·mol—1、P—O b kJ·mol—1、P="O" c kJ·mol—1、O=O d kJ·mol—1。根据下图示的分子结构和有关数据估算该反应的△H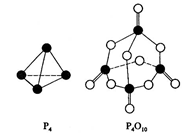
其中正确的是:
| A.(4a+5d-4c-12b)kJ·mol—1 |
| B.(4c+12b-4a-5d)kJ·mol—1 |
| C.(4c+12b-6a-5d)kJ·mol—1 |
| D.(6a+5d-4c-12b)kJ·mol—1 |