为了测定酸碱反应的中和热,计算时至少需要的数据是
①酸的浓度和体积;②碱的浓度和体积;③比热容;④反应后溶液的质量;⑤生成水的质量;⑥前后温度的变化;⑦操作所需时间
| A.①②④⑥ | B.③④⑤⑥ |
| C.①③④⑤ | D.全部 |
下列各装置中都盛有0.1 mol·Lˉ1的NaCl溶液,放置一定时间后,锌片的腐蚀速率由快到慢的顺序是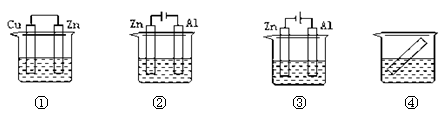
| A.③①④② | B.②①④③ | C.①②③④ | D.①②④③ |
下列说法正确的是
| A.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
| B.铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
| C.铅蓄电池放电时的负极和充电时的阳极均发生还原反应 |
| D.在潮湿的碱性环境中,金属的电化学腐蚀主要是析氢腐蚀 |
某反应:A="==B" + C 在室温下不能自发进行,在高温下能自发进行,对该反应过程的焓变(△H)、熵变(△S)的判断正确的是
| A.△H<0、△S>0 |
| B.△H>0、△S<0 |
| C.△H>0、△S>0 |
| D.△H<0、△S<0 |
下列设备工作时,将化学能转化为热能的是
在化学反应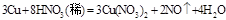 中,当有1.5molCu被氧化时
中,当有1.5molCu被氧化时
| A.有2mol硝酸被还原 |
| B.标准状况下有22.4L气体生成 |
| C.转移6mol电子 |
| D.有8mol硝酸参加反应 |