如图曲线a和b是盐酸与氢氧化钠相互滴定的滴定曲线,下列叙述正确的是
| A.盐酸的物质的量浓度为1 mol·L-1 |
| B.P点时恰好完全反应,溶液呈中性 |
| C.曲线a是盐酸滴定氢氧化钠的滴定曲线 |
| D.酚酞不能用作本实验的指示剂 |
在密闭容器中,对于反应N2+3H2 2NH3(g),N2、H2起始分别为10mol、30mol,达平衡时H2的转化率为25%,若从NH3开始反应,在相同条件下,欲使平衡时各成分的体积分数与前者相同,则起始时NH3的物质的量及NH3的转化率为()
2NH3(g),N2、H2起始分别为10mol、30mol,达平衡时H2的转化率为25%,若从NH3开始反应,在相同条件下,欲使平衡时各成分的体积分数与前者相同,则起始时NH3的物质的量及NH3的转化率为()
| A.15mol;25% | B.20mol;50% | C.20mol;75% | D.40mol;80% |
可逆反应2SO2+O2 2SO3正反应速率分别用υ(SO2)、υ(O2)、υ(SO3)[mol/(L·min)]表示,逆反应速率分别用υ'(SO2)、υ'(O2)、υ'(SO3)、[mol/(L·min)]表示。当反应达到化学平衡时,正确的关系是()
2SO3正反应速率分别用υ(SO2)、υ(O2)、υ(SO3)[mol/(L·min)]表示,逆反应速率分别用υ'(SO2)、υ'(O2)、υ'(SO3)、[mol/(L·min)]表示。当反应达到化学平衡时,正确的关系是()
| A.υ(O2)=υ(SO2)=υ(SO3) | B.υ(SO3)=υ'(SO2) |
| C.υ'(O2)=1/2υ'(SO2) | D.υ'(SO2)=υ'(SO3)=υ'(O2) |
X、Y、Z三种气体,当X和Y按1∶2的物质的量之比混合并通入密闭容器进行反应:X+2Y 2Z,当达到化学平衡时,反应物总物质的量与生成物总物质的量相等,此时x的转化率是( )
2Z,当达到化学平衡时,反应物总物质的量与生成物总物质的量相等,此时x的转化率是( )
| A.70% | B.60% | C.50% | D.40% |
.对可逆反应来说,使用催化剂的作用是( )
| A.提高反应物的平衡转化率 |
| B.以同样程度改变正逆反应的速度 |
| C.增大正反应速度,减小逆反应速度 |
| D.改变平衡混合物的组成 |
在高温下,反应2HBr(g)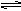 H2(g)+Br2(g);△H>0,达化学平衡时,要使混合气体的颜色加深,可采取的方法是( )
H2(g)+Br2(g);△H>0,达化学平衡时,要使混合气体的颜色加深,可采取的方法是( )
| A.减小压强 | B.缩小体积 |
| C.升高温度 | D.增大氢气的物质的量浓度 |