在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法正确的是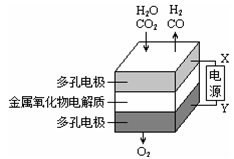
| A.X是电源的正极 |
| B.阴极的反应式是:H2O+2eˉ=H2+O2ˉ、CO2+2eˉ=CO+O2ˉ |
C.总反应可表示为:H2O+CO2 H2+CO H2+CO |
| D.阴、阳两极生成的气体的物质的量之比是1︰1 |
工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下: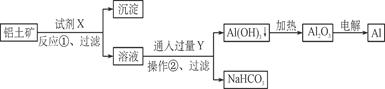
下列叙述正确的是
| A.试剂X可以是氢氧化钠溶液,也可以是盐酸 |
| B.反应①过滤后所得沉淀为氢氧化铁 |
| C.图中所示转化反应都不是氧化还原反应 |
| D.反应②的化学方程式为NaAlO2+CO2+2H2O===Al(OH)3↓+NaHCO3 |
下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象相同的是
| A.Na2CO3和HCl | B.AlCl3和NaOH |
| C.NaAlO2和H2SO4 | D.NaHCO3和Ba(OH) 2 |
下列说法正确的是(NA为阿伏加德罗常数的值)
| A.NA个Fe(OH)3胶体粒子的质量为107g |
| B.8.0 gCu2S和CuO的混合物中含有铜原子数为0.1NA |
| C.标准状况下,2.24 L Cl2溶于水中达到饱和,可得到HClO分子的数目是0.1NA |
| D.2.3gNa与氧气完全反应,反应中转移的电子数介于0.1 NA到0.2 NA之间 |
下列说法正确的是
| A.碱金属原子均易失去最外层电子达8电子稳定结构,故碱金属原子表现出较强还原性 |
| B.在Al(OH)3胶体中逐滴加入Ba(OH)2溶液至过量,先出现沉淀,后沉淀溶解 |
| C.某化合物在无色的酒精灯火焰上灼烧,焰色为黄色,则该化合物一定为含钠元素的盐 |
| D.由于水、苯和四氯化碳均为无色透明液体,所以水不能区分苯和四氯化碳 |
分子式为C5H12O2的二元醇有多种同分异构体,其中主链上碳原子数为3的同分异构体数目为m,主链上碳原子数为4的同分异构体数目为n。下列各组数据中m和n均正确的选项是(不包括同一个碳原子上连接两个羟基的化合物)
| A.m=1,n=6 | B.m=2,n=6 | C.m=1,n=7 | D.m=2,n=7 |