标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为c mol/L,则下列选项不正确的是
| A.ρ=(17V+22400 )/ (22.4+22.4V) | B.用水稀释该溶液,OH—的物质的量增加 |
| C.该溶液中共有6种微粒 | D.c=1000Vρ/(17V+22400) |
人体血液里存在重要的酸碱平衡: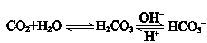 ,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
| c(HCO3-) ∶c(H2CO3) |
1.0 |
17.8 |
20.0 |
22.4 |
| pH |
6.10 |
7.35 |
7.40 |
7.45 |
下列说法不正确的是
A.正常人体血液中,HCO3-的水解程度大于电离程度
B.人体血液酸中毒时,可注射NaHCO3溶液缓解
C.pH=7.00的血液中,c(H2CO3)<c(HCO3-)
D.pH=7.40的血液中,HCO3-的水解程度一定大于H2CO3的电离程度
某溶液中含大量NH4+、Na+、HCO3-、CO32-、CH3COO-离子,其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)
| A.Na+ | B.CO32-、NH4+ | C.CH3COO- | D.CH3COO-、Na+ |
用如图所示装置进行实验,下列叙述不正确的是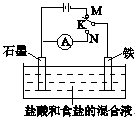
| A.K与N连接时,铁被腐蚀 |
| B.K与N连接时,石墨电极产生气泡 |
| C.K与M连接时,一段时间后溶液的pH增大 |
| D.K与M连接时,石墨电极反应:4OH—-4e—=2H2O+O2↑ |
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素。其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图。下列说法正确的是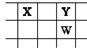
| A.五种元素中,原子半径最大的是W |
| B.Y的简单阴离子比W的简单阴离子还原性强 |
| C.Y与Z形成的化合物都可以和盐酸反应 |
| D.Z与Q形成的化合物水溶液一定显酸性 |
用黄色的FeCl3溶液分别进行下列实验,解释或结论不正确的是
| 实验 |
现象 |
解释或结论 |
|
| A |
加入FeCl3固体 |
溶液变成红褐色 |
FeCl3的水解程度变大 |
| B |
加入等体积水 |
溶液颜色变浅 |
c(Fe3+)变小 |
| C |
加入足量Fe粉 |
溶液颜色变浅绿色 |
2Fe3++ Fe=3Fe2+ |
| D |
将FeCl3溶液微热 |
溶液变成红褐色 |
水解反应ΔH>0 |