常温下,向0.1 mol/L的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验时不同阶段的溶液,下列有关说法中不正确的是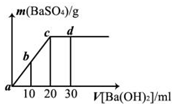
| A.溶液的pH:a<b<c<d |
| B.溶液的导电能力:a>b>d>c |
| C.a、b溶液呈酸性 |
| D.c、d溶液呈碱性 |
下列各组离子在指定溶液中能大量共存的是
①常温下,c(H+)/c(OH-)=1×10-12的溶液:K+、AlO2-、CO32-、Na+
②加入苯酚显紫色的溶液:K+、NH4+、Cl-、I-
③中性溶液:Fe3+、Al3+、NO3-、SO42-
④使pH试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl-
⑤无色溶液中:K+、Al3+、NO3-、HCO3-
A.② ③ ③ |
B.①③ | C.① | D.①④⑤ |
1L稀硝酸和稀硫酸的混合溶液,其溶质的物质的量浓度分别为0.1mol/L 和0.4mol/L。若向该混合溶液中加入足量的铜粉。则最多能溶解铜粉的质量为
| A.2.4 g | B.3.2 g | C.6.4 g | D.9.6 g |
下表各组物质中,物质之间不可能实现如图所示转化的是
| 选项 |
X |
Y |
Z |
M |
| A |
Al3+ |
Al(OH)3 |
AlO2- |
NaOH |
| B |
Fe |
FeCl2 |
FeCl3 |
Cl2 |
| C |
NaOH |
Na2CO3 |
NaHCO3 |
CO2 |
| D |
NH3 |
NO |
NO2 |
O2 |
某不纯的烧碱样品,含Na2CO3 3.8%(质量百分含量)、H2O 5.8%、NaHCO3 0.004%。取m g样品溶于40 mL 2 mol·L-1的盐酸后,并用 2 mol·L-1 NaOH溶液中和剩余的酸,在蒸发后可得干燥的固体的质量为
| A.4.68 g | B.5.58 g | C.2.34 g | D.2.34 mg |
已知:2BrO3- +Cl2="Br2" +2ClO3-;5Cl2 +I2 +6H2O ="2HIO3" +10HCl;ClO3- +5Cl- +6H+ =3Cl2+3H2O下列物质氧化能力强弱顺序为
| A.ClO3->BrO3->IO3->Cl2 | B.BrO3->Cl2>ClO3->IO3- |
| C.BrO3->ClO3->Cl2>IO3- | D.Cl2>BrO3->ClO3->IO3- |