常温时,以下4种溶液pH最小的是
| A.0.01mol/L醋酸溶液 |
| B.0.02mol/L醋酸与0.02mol/LNaOH溶液等体积混合液 |
| C.0.03mol/L醋酸与0.01mol/LNaOH溶液等体积混合液 |
| D.pH = 2的盐酸与pH = 12的NaOH溶液等体积混合液 |
下列说法错误的是
A.稀土元素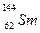 与 与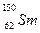 是同一种核素 是同一种核素 |
| B.Al、Al2O3、Al(OH)3都可溶于NaOH溶液和盐酸中 |
| C.甲烷燃烧放热,表明了反应物的总能量大于生成物的总能量 |
| D.向豆浆中加入硫酸钙制豆腐,是利用了胶体的聚沉性质 |
下列说法错误的是
| A.用煤制取甲醚(CH3OCH3)替代石油,可以缓解我国石油的供需矛盾 |
| B.医疗上用的“钡餐”其成分是氯化钡 |
| C.氮化硅陶瓷、通讯光缆等都是新型无机非金属材料 |
| D.利用风能、生物能发电,将火力发电用煤进行脱硫处理,有利于环保 |
如图:X为铁棒,Y为铜棒,当K闭合后,下列有关分析不正确的是( )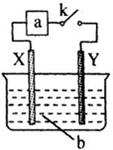
| A.当a为电流表,b为浓硝酸时:Y为负极 |
B.当a为电流表,b为稀硫酸时:X电极反应为: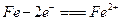 |
C.当a为直流电源,b为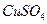 溶液时:X、Y两电极附近的 溶液时:X、Y两电极附近的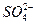 浓度相等 浓度相等 |
| D.当a为直流电源,b为NaOH溶液,X极附近产生白色沉淀时:电子从X极流入a |
下列实验过程中产生的现象与对应图形相符合的是()
下列叙述正确的是()
A.10 mL 0.1 mol/L NH4Cl溶液与5 mL 0.2 mol/L NaOH溶液混合:
B.0.1mol/L PH为4的NaHB的溶液中,c(HB—)> c (H2B)> c (B2 —)
—)
C.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、AlO2-、SO42-
D.相同条件下,pH=5的①NH4Cl溶液、②CH3COOH溶液、③稀盐酸溶液中由水电离出的c (H+):①>②>③