某纯碱厂技术科的人员对该厂纯碱样品的质量进行检验。其中能够说明纯碱样品中可能含有杂质(NaHCO3)的实验是
①样品溶于水,并加入足量的澄清石灰水,变浑浊
②样品溶于水,并加入足量的BaCl2溶液,变浑浊
③样品在硬质试管中加强热,排出的气体通入澄清石灰水,变浑浊
④向样品中滴加稀盐酸,排出的气体通入澄清石灰水,变浑浊
| A.①②③ | B.①③④ | C.①②④ | D.只有③ |
从下列事实所得出的相应结论正确的是( )
| 实验事实 |
结 论 |
|
| ① |
A元素的原子半径比B元素的原子半径大 |
周期表中A位于B的下一周期 |
| ② |
将CO2通入到Na2SiO3溶液中产生白色浑浊(H2SiO3) |
酸性: H2CO3>H2SiO3 |
| ③ |
将燃烧的镁条放入CO2中能继续燃烧 |
还原性:Mg>C |
| ④ |
常温下白磷可自燃而氮气须在放电时才与氧气反应 |
非金属性:P>N |
| ⑤ |
某无色溶液中加入硝酸酸化的硝酸钡溶液产生白色沉淀 |
原溶液一定有SO42- |
| A.③④⑤ | B.①②③⑤ | C.②③ | D.全部 |
右图为元素周期表短周期的一部分。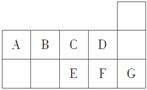
关于A~G七种元素的叙述正确的是( )
A.E、F、G形成的单质中都含有共价键
B.形成的简单阴离子半径:E>F>C>D
C.B、C、D三种元素的氢化物的稳定性依次减弱
D.A、B、E的氢化物都能跟HNO3发生化合反应
现代无机化学对硫氮化合物的研究是最为活跃的领域之一。如图是已经合成的最著名的硫氮化合物的分子结构。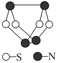
下列说法正确的是( )
| A.该物质的分子式为SN |
| B.该物质的分子中所有原子的最外层都达到8电子稳定结构 |
| C.含有1 mol的该物质的微粒中含有共价键为8NA |
| D.该物质与化合物S2N2互为同位素 |
下列各项中表达正确的是( )
A.NH3分子的电子式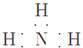 |
B.CH4分子的比例模型: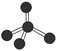 |
C.O原子的结构示意图: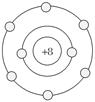 |
| D.N2的结构式:N≡N |
下列叙述正确的是( )
| A.同主族元素从上到下,元素原子得电子能力逐渐减弱,表现在氢化物的稳定性逐渐减弱,熔沸点逐渐升高 |
| B.除稀有气体元素外,第三周期元素的原子半径不一定比第二周期元素的原子半径大 |
| C.化合反应都是放热反应,分解反应都是吸热反应。因此化合反应都形成新化学键,分解反应都破坏旧化学键 |
| D.在主族元素中,最外层电子数少的元素原子一定比最外层电子数多的元素原子失电子能力强 |