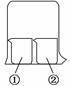
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是
| |
①中的物质 |
②中的物质 |
预测①的现象 |
| A |
淀粉KI溶液 |
浓硝酸 |
无明显变化 |
| B |
酚酞溶液 |
浓盐酸 |
无明显变化 |
| C |
AlCl3溶液 |
浓氨水 |
有白色沉淀 |
| D |
湿润红纸条 |
饱和氯水 |
红纸条褪色 |
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g) 4NO2(g)+ O2(g) △H >0 ,T1温度下的部分实验数据为
4NO2(g)+ O2(g) △H >0 ,T1温度下的部分实验数据为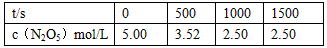
下列说法不正确的是
| A.500s内N2O5分解速率为2.96×10-3 mol/(L·s) |
| B.T1温度下的平衡常数为K1=125,1000s时转化率为50% |
| C.其他条件不变时,T2温度下反应到1000s时测得N2O5(g)浓度为2.98 mol/L,则T1<T2 |
| D.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1 >T2,则K1> K2 |
已知某反应中反应物与生成物有:KIO3、Na2SO3、H2SO4、I2、K2SO4、H2O 和未知物X。下列说法中不正确的是
| A.该未知物X为Na2SO4 |
| B.该反应的氧化剂是KIO3 |
| C.该反应中,发生氧化反应的过程是KIO3→I2 |
| D.由反应可知还原性强弱顺序为:Na2SO3>I2 |
下列各项叙述中,正确的是
| A.所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同 |
| B.价电子排布式为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |
| C.镁原子由1s22s22p63s2 →1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
| D.24Cr原子的电子排布式是1s22s22p63s23p63d44s2 |
若不断地升高温度,实现"雪花→水→水蒸气→氧气和氢气"的变化。在变化的各阶段被破坏的粒子间主要的相互作用依次是
| A.氢键;分子间作用力;非极性键 | B.氢键;氢键;极性键 |
| C.氢键;极性键;分子间作用力 | D.分子间作用力;氢键;非极性键 |
常温下,下列各组物质中,Y既能与X反应,又能与Z反应的是
| 选项 |
X |
Y |
Z |
| ① |
N2 |
Mg |
CO2 |
| ② |
KOH溶液 |
SiO2 |
氢氟酸 |
| ③ |
O2 |
N2 |
H2 |
| ④ |
稀硝酸 |
Fe |
FeCl3溶液 |
A.①② B.①③ C.②③ D.②④