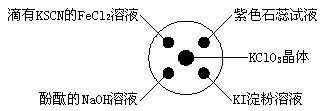
已知:KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O。如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是
| 选项 |
实验现象 |
结论 |
| A |
滴有KSCN的FeCl2溶液变红 |
Cl2具有还原性 |
| B |
滴有酚酞的NaOH溶液褪色 |
Cl2具有酸性 |
| C |
紫色石蕊溶液先变红后褪色 |
Cl2具有漂白性 |
| D |
KI淀粉溶液变蓝色 |
Cl2具有氧化性 |
据报道,1991~1996年人类发现和创造的化合物已有1 000多万种,这正好相当于到1990年以前人类在100多万年以来已知物质的总量,此外,关于物质的信息量也剧增,请推断,新发现和新创制的物质主要是( )
| A.放射性同位素 | B.无机物 |
| C.有机化合物 | D.烃类物质 |
下列说法中,不正确的是( )
| A.大多数有机物难溶于水,易溶于汽油、苯等有机溶剂 |
| B.有机物的熔点低,受热易分解,都能燃烧 |
| C.有机物都是非电解质,不易导电 |
| D.有机物的化学反应比较复杂,一般较慢,且常伴有副反应发生 |
金属晶体和离子晶体是两种重要的晶体类型。下列关于它们的说法中,正确的是( )
| A.金属晶体和离子晶体(固态时)都能导电 |
| B.在镁晶体中,1个Mg2+只与2个价电子存在强烈的相互作用 |
| C.金属晶体和离子晶体都可采取“紧密堆积”方式 |
| D.金属晶体和离子晶体中分别存在金属键和离子键等强烈的相互作用,很难断裂,因而都具有延展性 |
物质有多种多样的聚集状态,下列有关说法错误的是( )
| A.组成纳米材料的结构粒子是纳米量级的原子团 |
| B.二氧化硅晶体中,每个Si原子与4个氧原子形成共价键,故晶体中硅、氧原子个数比为1∶4 |
| C.NaI与NaCl晶体比较,NaI的离子间距更大,晶格能的绝对值更小,熔点更低 |
| D.等离子体中的微粒带有电荷且能自由运动,使等离子体具有很好的导电性 |
关于晶体与化学键关系的下列说法中,正确的是( )
| A.离子晶体中一定存在共价键 |
| B.原子晶体中可能存在离子键 |
| C.金属晶体中存在离子,但却不存在离子键 |
| D.分子晶体中一定存在共价键 |