已知热化学方程式:2H2(g)+O2(g)=2H2O(g)△H1=-483.6kJ/mol,则对于热化学方程式:2H2O(l)=2H2(g)+O2(g)△H2=b,下列说法正确的是
| A.热化学方程式中化学计量数表示分子个数 |
| B.该反应的△H2=+483.6 kJ/mol |
| C.形成2mol H-O键放出能量比断2mol H-H及1mol O=O键所需能量多483.6kJ |
| D.|△H2|>|△H1| |
实验室可用加热2KClO3分解的方法制取氧气,反应中使用MnO2作为催化剂,反应后从剩余物中回收二氧化锰的操作顺序正确的是(已知MnO2为黑色难溶于水的固体)
| A.溶解、过滤、蒸发、洗涤 | B.溶解、过滤、洗涤、干燥 |
| C.溶解、蒸发、洗涤、过滤 | D.溶解、洗涤、过滤、加热 |
下列实验装置图中没有涉及气体压强原理的是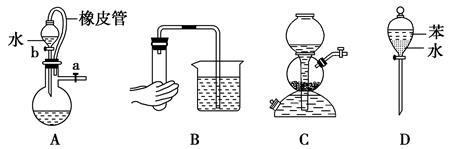
已知乙酸乙酯(C4H8O2)是一种无色液体,不溶于水,密度小于1 g·mL-1,沸点约为55 ℃。要从水与乙酸乙酯的混合物中将乙酸乙酯分离出来,下列方法中最简便的是
| A.蒸馏 | B.分液 | C.过滤 | D.蒸发 |
下列仪器:①烧杯、②坩埚、③锥形瓶、④蒸发皿、⑤试管、⑥烧瓶、⑦表面皿,用酒精灯加热时,需要垫石棉网的是
| A.②④⑤ | B.①⑥⑦ | C.③④⑥ | D.①③⑥ |
在汽车加油站见到的油罐车上,所贴的危险化学品标志是