化学反应N2+3H2 2NH3的能量变化下图所示,该反应的热化学方程式是
2NH3的能量变化下图所示,该反应的热化学方程式是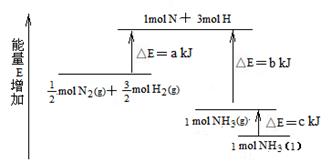
A.N2(g)+3H2(g)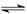 2NH3(1);△H=2(a-b-c)kJ·mol-1 2NH3(1);△H=2(a-b-c)kJ·mol-1 |
B.N2(g)+3H2(g)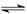 2NH3(g);△H=2(b-a)kJ·mol-1 2NH3(g);△H=2(b-a)kJ·mol-1 |
C.1/2N2(g)+ 3/2H2(g)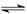 NH3(1);△H=(b+c-a)kJ·mol-1 NH3(1);△H=(b+c-a)kJ·mol-1 |
D.1/2N2(g)+3/2H2(g)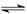 NH3(g);△H=(a+b)kJ·mol-1 NH3(g);△H=(a+b)kJ·mol-1 |
暴露在空气中不易变质的是
| A.钠 | B.氯化钠 | C.氧化钙 | D.氢氧化钠 |
工业上用洗净的废铜作原料来制备硝酸铜。为了节约原料和防止污染环境,宜采取的方法是
不属于氧化还原反应的是
A.2Al+Fe2O3 2Fe+Al2O3 2Fe+Al2O3 |
B.2Mg+CO2 2MgO+C 2MgO+C |
C.N2+3H2 2NH3 2NH3 |
D.SiO2+CaO CaSiO3 CaSiO3 |
下列叙述正确的是
A.NaOH 、Mg(OH)2、Al(OH)3碱性依次减弱
B.Na 、Mg、Al原子半径依次增大
C.H2SO4、H3PO4、HClO4酸性依次增强
D.HCl、HBr、HI稳定性依次增强
下列各组中的离子或分子,能较大量共存同一溶液中的是
| A.Fe2+、Cl2、I— | B.Fe3+、OH-、NH4+ |
| C.H+、SO42—、OH— | D.K+、NO3-、Cu2+ |