在一定条件下,2体积XY3气体分解生成1体积Y2和2体积气态化合物甲。则甲的化学式为
| A.XY | B.XY2 | C.XY3 | D.X2Y3 |
广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果都是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质。根据上述观点,下列说法错误的是( )
| A.CaO2的水解产物是Ca(OH)2和H2O2 |
| B.(CH3)3COMgBr的水解产物是(CH3)3COH和Mg(OH)Br |
| C.PCl3的水解产物是PH3和HClO |
| D.A1(C2H5)3的水解产物是Al(OH)3与C2H6 |
在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g) Fe(s)+CO2(g)△H="a" kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是( )
Fe(s)+CO2(g)△H="a" kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是( )
| A.若生成1 mol Fe,则吸收的热量小于a kJ |
| B.若升高温度,正反应速率加快,逆反应速率减慢,则化学平衡正向移动 |
| C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| D.达到化学平衡状态时,若c(CO)="0.100" mol/L,则c(CO2)="0.0263" mol/L |
如图为一恒压容器。在恒定温度下,将1 mol N2和3 mol H2混合后由A口快速充入容器,封闭A。反应N2+3H2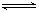 2NH3在t1时刻达到平衡;t2时刻再从A口快速充入一定量NH3,封闭A;t3时刻重新达到平衡至t4。在0→t4时间内混合气中NH3的体积分数(纵坐标)随时间(横坐标)变化的曲线正确的是( )
2NH3在t1时刻达到平衡;t2时刻再从A口快速充入一定量NH3,封闭A;t3时刻重新达到平衡至t4。在0→t4时间内混合气中NH3的体积分数(纵坐标)随时间(横坐标)变化的曲线正确的是( )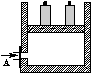

实验室欲配制一种仅含四种离子(不考虑来源于水电离的离子)的溶液,且溶液中四种离子的浓度均为1mol/L,能达到此目的的是( )
| A.Na+、K+、Br-、NO3- | B.Ba2+、Mg2+、SO42-、Cl- |
| C.ClO-、I-、K+、Na + | D.H+、K+、Cl-、CO32- |
常温下,取0.3 mol/LHY溶液与0.3 mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH = 9,则下列说法(或关系式)正确的是( )
| A.混合溶液中由水电离出的c(OH-)=10-9 mol/L |
| B.溶液中离子浓度由大到小的顺序为 c(Y-)> c(Na+) > c(OH-)>c(H+) |
| C.c(OH-)-c(HY)=c(H+)=1×10-9mol/L |
| D.c(Na+)=c(Y¯)+c(HY) =0.3 mol/L |