下列对“改变反应条件,导致化学反应速率改变”的原因描述不正确的是
| A.增大反应物的浓度,活化分子百分数增加,反应速率加快 |
| B.增大气体反应体系的压强,单位体积中活化分子数增多,气体反应速率加快 |
| C.升高反应的温度,活化分子百分数增加,有效碰撞的几率提高,反应速率增大 |
| D.催化剂通过改变反应路径,使反应所需的活化能降低,反应速率增大 |
生铁和钢的主要区别是()
| A.生铁和钢的主要成分都是铁,但二者的含碳量不同,性能也不同。 |
| B.生铁和钢都是碳的合金 |
| C.生铁就是含杂质较多的钢,钢就是含杂质较少的生铁。 |
| D.生铁是混合物,钢是纯净物 |
高温下丁烷完全裂化生成四种气体,将混合气体用溴水处理后,剩余气体的平均分子质量为21.6,则原四种混合气体的平均分子质量是
| A.21.6 | B.27.6 | C.29 | D.36.4 |
在H2SO4、K2SO4、Al2 (SO4)3和明矾[KAl(SO4)2·12H2O]的混合溶液中,H+的浓度为0.2mol/L,SO42-的浓度为0.5mol/L,当加入等体积0.6mol/L KOH溶液时,生成的沉淀恰好完全溶解。则反应后溶液中K+的浓度约为
| A.0.225mol/L | B.0.25mol/L | C.0.45mol/L | D.0.55mol/L |
对于反应3Cl2+6NaOH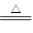 5NaCl+NaClO3+3H2O,以下叙述正确的是
5NaCl+NaClO3+3H2O,以下叙述正确的是
| A.Cl2是氧化剂,NaOH是还原剂 |
| B.当有6.72L Cl2反应时,转移电子物质的量为0.5mol |
| C.氧化剂得电子总数与还原剂失电子总数之比为1∶1 |
| D.被氧化的氯原子和被还原的氯原子的物质的量之比为5∶1 |
下列根据实验事实得出的结论正确的是
| 实 验 事 实 |
结 论 |
|
| A |
加热的铝箔熔化,但液态的铝不滴落 |
熔点:氧化铝>铝 |
| B |
溶液中加入盐酸酸化的BaCl2溶液有白色沉淀生成 |
该溶液中一定含有SO42- |
| C |
碳酸钠溶液能使酚酞试液变红 |
碳酸钠溶液呈碱性 |
| D |
常温下,铜与冷的浓H2SO4不反应 |
铜与浓硫酸发生钝化 |