向含Fe2+、Br-、I-各0.1mol的溶液中通入标准状况下的Cl2,通入Cl2的体积和溶液中某种离子的物质的量的关系如图,下列说法中正确的是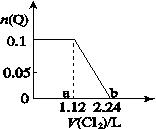
| A.Q是I- |
| B.Q是Br- |
| C.ab区间的反应:2Fe2++Cl2===2Fe3++2Cl- |
| D.b点时溶液中只有Cl- |
有规律称:强酸溶液每稀释 10倍 pH增加 1,强碱溶液每稀释 10倍 pH减小 1,但此规律有一定的局限性。试问将 pH = 3的 H2SO4(aq)稀释 105倍,其 pH约为
| A.8 | B.7 | C.2 | D.3 |
按下述实验方法制备气体,合理又实用的是
| A.锌粒与稀HNO3反应制备H2 |
| B.向饱和NaCl溶液中滴加浓H2SO4制备HCl |
| C.亚硫酸钠与浓H2SO4反应制备SO2 |
| D.大理石与浓H2SO4反应制备CO2 |
下列材料中最不适宜制造储存浓硫酸的容器的是
| A.铁 | B.铝 | C.铜 | D.陶瓷 |
为了实现我国政府于1997年12月21日对淮河流域环境的治理,某甲、乙相邻的工厂做了横向联合,已知两厂排放的污水经处理后,只溶有浓度较大的Ag+、Ba2+、Fe3+、Na+、Cl-、 、
、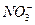 、OH-中的各不同的4种离子,若单独排放仍会污染环境,如将两厂的污水按适当的比例混合,沉淀后污水变成无色澄清的NaNO3溶液排出,则污染程度会大为降低,你认为下列判断正确的是
、OH-中的各不同的4种离子,若单独排放仍会污染环境,如将两厂的污水按适当的比例混合,沉淀后污水变成无色澄清的NaNO3溶液排出,则污染程度会大为降低,你认为下列判断正确的是
A. 和 和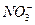 可存在于同一工厂 可存在于同一工厂 |
B.Cl-和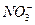 一定在不同的工厂 一定在不同的工厂 |
| C.Ag+和Na+可能在同一工厂 |
D.Fe3+与 存在于同一工厂 存在于同一工厂 |
检验SO2中是否有CO2,应采用的方法是
| A.通过石灰水 |
| B.通过品红溶液 |
| C.先通过小苏打溶液,再通过石灰水 |
| D.先通过KMnO4酸性溶液,再通过石灰水 |