反应A(g)+B(g)⇌C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题。
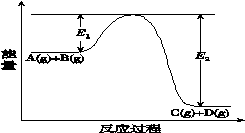
①图中E1代表的意义是_____________________。
该反应是______________反应(填“吸热”或“放热”)。反应热ΔH的表达式为________________。
②当反应达到平衡时,升高温度,A的转化率______________(填“增大”“减小”或“不变”)。
(2)800 ℃时,在2 L密闭容器内充入0.50 mol NO和0.25 mol O2,发生如下反应:2NO(g)+O2(g)===2NO2(g)ΔH<0。体系中,n(NO)随时间的变化如下表:
| t/s |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)/mol |
0.50 |
0.35 |
0.28 |
0.25 |
0.25 |
0.25 |
①能说明该反应已达到平衡状态的是______________。
A.v(NO2)正=v(O2)逆 B.容器内压强保持不变
C.v(NO)逆=2v(O2)正 D.容器内气体颜色不变
②能使该反应的反应速率增大,且平衡向正反应方向移动的措施是______________。
A.适当升高温度 B.缩小反应容器的体积
C.增大O2的浓度 D.选择高效催化剂
将7.1g Na2SO4放人足量水中完全溶解,得到200g Na2SO4溶液,则该溶液中含有溶质Na2S04的物质的量为_________mol,溶液中Na+的物质的量为________mol,SO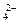 的物质的量为_________mol。此溶液中Na2SO4的质量分数为_________。
的物质的量为_________mol。此溶液中Na2SO4的质量分数为_________。
(1)过氧化钠可用作于制氧剂,写出过氧化钠与二氧化碳反应的化学方程式
(2)工业上制取漂白粉的化学方程式为____________________。漂白粉露置于空气中失效的原因是(用化学方程式表示):
①_________,
②___________________。
(1)新制备的氯水显__________色,说明氯水中有__________(填分子式)分子存在。
(2)向氯水中滴加几滴AgNO3溶液,立即有__________生成,说明氯水中有__________(填化学式)存在,反应的化学方程式为__________________________。
(3)氯水光照后颜色变浅,并放出________色的气体。
新切开的金属钠,切面呈________色,在空气中很快变暗,有关的化学方程式是________.将小块金属钠投入盛有水的烧杯里,钠熔化成闪亮的小球,说明________.向烧杯中滴加酚酞试液,溶液呈________色,说明________,反应的化学方程式为_____
A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。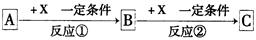 ,试回答:
,试回答:
⑴若X是强氧化性单质,则A不可能是_______________(可多选)。
A. S B. N2 C. Na D. Mg E. Al
⑵若A、B、C为含有同种金属元素的无机化合物,X为强电解质,A溶液与C溶液反应可生成B,则B的化学式可能为________,X的化学式可能为(写出不同类物质)______或__________,反应①的离子方程式为__________或_____________________。
⑶若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则A的电子式为______;C溶液在贮存时应加入少量X,理由是(用离子方程式表示)____________,检验此C溶液中金属元素价态的操作方法是___________________。