容积固定的密闭容器中存在如下反应:A(g)+3B(g) 2C(g) △H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
2C(g) △H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
下列判断一定错误的是
①图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
②图Ⅱ研究的是压强对反应的影响,且甲的压强较高
③图Ⅱ研究的是温度对反应的影响,且甲的温度较高
④图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
| A.①② | B.①③ | C.②④ | D.③④ |
核电荷数小于18的某元素X,某原子核外电子层数为a,最外层电子数为(2a+1)。下列有关元素X的说法中,不正确的是
| A.元素X的原子核内质子数为(2a2-1) |
| B.元素X的原子半径一定小于钠的原子半径 |
| C.由元素X形成的某些化合物,可能具有杀菌消毒的作用 |
| D.元素X形成的简单离子,各电子层的电子数均达到2n2个(n表示电子层数) |
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。下列说法正确的是
A.元素A、B组成的化合物可能是NH3
B.一定条件下,元素C、D的最高价氧化物对应的水化物之间不能发生反应
C.C、D、E的半径:C>D>E
D.化合物AE与CE具有相同类型的化学键
下列各组元素中,按最高正价递增顺序排列的是
A.Na、Mg、Al、S B.C、N、O、F
C.F、Cl、Br、ID.Li、Na、K、Rb
某元素的一种同位素X原子的质量数为A,含N个中子,它与1H原子组成HmX分子,在ag HmX分子中含质子的物质的量是
A.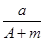 (A+N+m)mol (A+N+m)mol |
B. (A-N)mol (A-N)mol |
C.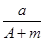 ( A-N)mol ( A-N)mol |
D.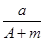 (A-N+m)mol (A-N+m)mol |
在一定条件下,RO3-与R-可发生反应:RO3-+5R-+6H+== 3R2+3H2O,下列关于R元素的叙述中,正确的是
| A.元素R位于周期表中第ⅤA族 |
| B.RO3-中的R只能被还原 |
| C.R2在常温常压下一定是气体 |
| D.若1 mol RO3-参与该反应,则转移的电子的物质的量为5 mol |