将一定质量的铁、氧化铁、氧化铜的混合物粉末放入100 mL 4.40 mol·L-1盐酸中,充分反应后产生896 mL H2(标准状况),残留固体1.28 g。过滤,滤液中无Cu2+。将滤液加水稀释到200 mL,测得其中c(H+)为0.400 mol·L-1。则原混合物中单质铁的质量是
| A.2.24 g | B.3.36 g | C.5.60 g | D.10.08 g |
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中A是组成有机物的必要元素,元素B的原子最外层电子数是其电子层数的3倍,元素D与A为同族元素,元素C与E形成的化合物CE是厨房 常用调味品。下列说法正确的是
常用调味品。下列说法正确的是
A.原子半径:C>D>A>B
B.C和E的单质可通过电解饱和的CE水溶液获得
C.C与B形成的两种化合物中化学键类型完全相同
D .A、D、E的最高价氧化物对应水化物的酸性逐渐增强
.A、D、E的最高价氧化物对应水化物的酸性逐渐增强
用NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.lmol Na2O2晶体中共含有4NA个离子 |
| B.常温常压下16gO2和O3混合气体含有NA个氧原子 |
| C.0.1mol AlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒 |
| D.17g的氢氧根离子中含有的电子数为9NA |
下列有关化学用语使用正确的是
A.CO2的电子式: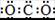 |
B.核内有8个中子的碳原子: |
C.F-离子结构示意图: |
D.HCN分子的结构式:H-C≡N |
化学在人类生活中扮演着重要角色,以下应用正确的是
| A.使用无磷洗衣粉,可彻底解决水体富营养化问题 |
| B.为改善食物的色、香、味并防止变质,可在其中加入大量食品添加剂 |
| C.研发高效低毒的农药,可降低作物的农药残留量 |
| D.天然药物无任何毒副作用,可长期服用 |
常温下,把pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,在所得溶液中离子浓度大小关系正确的是()
| A.c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | B.c(Na+)+c(H+)>c(CH3COO-)+c(OH-) |
C.c(CH3COO-)>c (Na+)>c(H+)=c(OH-) (Na+)>c(H+)=c(OH-) |
D.c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |