甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题:
(1)一定温度下,在一恒容的密闭容器中,由CO和H2合成甲醇:
CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
①下列情形不能说明该反应已达到平衡状态的是 (填序号)
A.每消耗1mol CO的同时生成2molH2
B.混合气体总物质的量不变
C.生成CH3OH的速率与消耗CO的速率相等
D.CH3OH、CO、H2的浓度都不再发生变化
②CO的平衡转化率(α)与温度、压强的关系如下图所示。

B、C两点的平衡常数K(B) K(C)(填“>”、“=”或“<”).
③某温度下,将2.0mol CO和6.0molH2充入2L的密闭容器中,达到平衡时测得c(CO)=0.25mol/L,CO的转化率= ,此温度下的平衡常数K= (保留二位有效数字)
(2)常温下,将V mL、0.20mol/L氢氧化钠溶液逐滴加入到20.00mL、0.20mol/L甲酸溶液中,充分反应,溶液pH=7,此时V 20.00(填“>”、“=”或“<”);当氢氧化钠溶液与甲酸溶液恰好完全反应时,溶液中所含离子浓度由大到小顺序__ _____
(3)温度650℃的熔融盐燃料电池,用(CO、H2)作反应物,空气与CO2的混合气体为正极反应物,镍作电极,用Li2CO3和Na2CO3混合物作电解质.该电池的正极反应式为
(4)己知:CH3OH、H2的燃烧热(△H)分别为﹣726.5kJ/mol、﹣285.8kJ/mol,则常温下CO2和H2反应生成CH3OH和H2O的热化学方程式是
X、Y、Z三元素的原子序数依次增大,三原子的核外最外层电子排布均为4s1。
(1)X元素组成的单质的晶体堆积模型为___________(填代号)。
a.简单立方堆积 b.体心立方堆积
c.六方最密堆积 d.面心立方最密堆积
(2)Y元素在其化合物中最高化合价为________;YO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断YO2Cl2是__________(填“极性”或“非极性”)分子。
(3)ZCl微溶于水,但能溶解在氯化钾的浓溶液中,原因 是。
(4)ZCl的晶胞结构如图所示,已知晶胞边长为a pm,密度为ρ g/cm3,则阿伏加德罗常数可表示为(列式表示)。
(5)已知ZnS的晶体结构与ZCl相似,下表列出了离子半径和熔点数据,解释ZnS和ZCl的熔点差异的主要原因。
| r(Zn2+) |
r(Z+) |
r(S2-) |
r(Cl-) |
熔点 |
|
| ZnS |
ZCl |
||||
| 74pm |
77pm |
184pm |
181pm |
1700℃ |
430℃ |
三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
(1)该反应的化学方程式为。
(2)N、F两种元素的氢化物稳定性比较,NH3HF(选填“>“或”<“)。
(3)N3- 被称为类卤离子,写出一种与N3-互为等电子体的分子的化学式,N3-的空间构型为。
(4)CaF2的晶胞结构如图,若该晶胞边长为a pm,晶胞中F-半径为b pm,则Ca2+ 半径的表达式为pm(列式表示)。
下表为元素周期表的一部分,其中编号代表对应的元素。
请回答下列问题: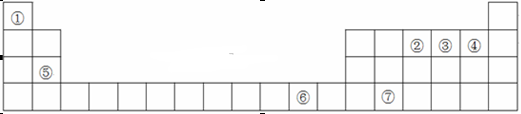
(1)写出元素⑦的基态原子的价电子排布式, 元素⑥位于元素周期表中区。
(2)元素②、③、④的第一电离能大小顺序是
(用元素符号表示)。
(3)在叶绿素a中含有元素⑤,下图是叶绿素a的部分结构,在该分子中C原子的杂化类型有,存在的化学键有。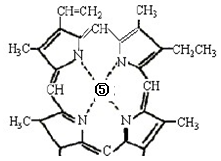
(4)②和⑥形成某种化合物的晶胞结构如图所示(每个球均表示1个原子,其中②显-3价),则其化学式为。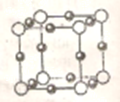
两种烃的衍生物A和B,所含碳、氢、氧的质量比均为6:1:4。完全燃烧0.1molA能生成3.6g水。B只含一个醛基,1.1gB与足量银氨溶液反应,可析出2.7gAg。
(已知Ag的相对原子质量为108)。通过计算回答以下问题:
(1)A和B的分子式分别为________________和_______________
(2)若B还能与酸发生酯化反应,且主链含3个碳原子,则其可能的结构简式有:
__________________________________________
含有苯环的化合物A有下列一系列变化关系,其中D能使FeCl3显紫色,E、F、G能发生银镜反应:且知,A在苯环上一溴代物只有二种
(1)A的结构简式________________________
(2)反应①—⑤中可看成取代反应的有__________________(填代号)
(3)反应⑤中浓硫酸的作用是_____________________
(4)写出下列反应方程式
B→D:__________________________________________
C+F→G:___________________________________________