(1)CH3-CH3→CH2=CH2+H2,有关化学键的键能如下:
| 化学键 |
C-H |
C=C |
C-C |
H-H |
| 键能(kJ/mol) |
414.4 |
615.3 |
347.4 |
435.3 |
计算该反应的反应热 (写出计算过程)
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H=-24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
(3)发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
已知:N2(g)+2O2(g)===2NO2(g) ΔH1=+67.7 kJ/mol
N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH2=-534 kJ/mol
试计算1 mol肼和二氧化氮完全反应时放出的热量为__________________kJ,写出肼与二氧化氮反应的热化学方程式:______________________
如图是A分子的球棍模型和B分子的比例模型,回答下列问题:
(1)A和B的关系是_____。
(2)写出A分子在催化剂存在条件下加热和氧气反应的化学方程式___________。
(3)写出B分子和金属钠反应的化学方程式_____________________。
(4)B在加热条件下能够和HBr发生反应生成溴乙烷,该反应类型是____________。
某烃A不能使溴水褪色,0.5 mol A完全燃烧时,得到1.5 mol H2O和67.2 L CO2(标准状况)。
(1)A的结构简式为___________________。
(2)根据下列条件写出有关反应的化学方程式。
①在催化剂FeCl3的作用下,A与Cl2反应生成B:________________。
②在催化剂作用下,A与H2反应生成C:__________。
甲烷、乙烯、苯、甲苯四种有机物中具有下列性质的是:
(1)不能与溴水反应,能使酸性高锰酸钾溶液褪色的是________________。
(2)在催化剂作用下能与纯溴反应,不能使酸性高锰酸钾溶液褪色的是________。
(3)见光能跟氯气反应,不能使酸性高锰酸钾溶液褪色的是________。
(4)在催化剂作用下加氢生成乙烷,加水生成酒精的是________。
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应。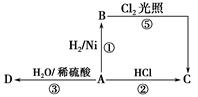
据图回答下列问题:
(1)写出A、C、D的结构简式:
A________,C________,D________。
(2)写出①②两步反应的化学方程式,并注明反应类型:
①________________________________(反应类型____________)。
②________________________________(反应类型____________)。
足球比赛中当运动员肌肉挫伤或扭伤时,队医会迅速对运动员的受伤部位喷射一种药剂——氯乙烷(沸点为12.27 ℃)进行局部冷冻麻醉应急处理。
(1)氯乙烷用于冷冻麻醉应急处理的原因是_______________________。
(2)制取CH3CH2Cl最好的方法是________。
| A.乙烷与氯气反应 | B.乙烯与氯气反应 | C.乙烷与HCl反应 | D.乙烯与HCl反应 |
(3)选择上述方法的理由是____________;制取发生反应的化学方程式为_________________________________________。