常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mLpH=14的溶液,然后用1mol•L-1的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是
| A.原合金质量为0.92g | B.图中V2为60 |
| C.沉淀的质量m为1.56g | D.OP段发生的反应为:OH-+H+═H2O |
下列关于化学反应限度的说法中正确的是()
| A.一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度 |
| B.当一个可逆反应达到平衡状态时,正向反应速率和逆向反应速率相等且等于零 |
| C.平衡状态时,各物质的浓度保持相等 |
| D.化学反应的限度不可以通过改变条件而改变 |
已知反应X+Y====M+N为吸热反应,对这个反应的下列说法中正确的是( )
| A.X的能量一定低于M的,Y的能量一定低于N的 |
| B.因为该反应为吸热反应,故一定要加热反应才能进行 |
| C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 |
| D.X和Y的总能量一定低于M和N的总能量 |
下列反应条件的控制中,不恰当的是()
| A.为了防止铁生锈,在其表面涂一层防锈油漆 |
| B.为防止火灾,在面粉厂、加油站等场所要严禁烟火 |
| C.为加快KClO3的分解速率,加入MnO2 |
| D.为加快H2O2的分解速率,把反应容器放到冷水中冷却 |
如图所示能够组成原电池,并且产生明显的电流的是( )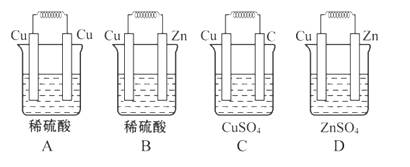
下列物质的电子式正确的是