下列实验能达到目的的是
| A.在容量瓶中加一定体积的水,再加入浓盐酸配制准确浓度的稀盐酸 |
| B.蒸馏操作时在蒸馏烧瓶中加入沸石以防止爆沸 |
| C.用玻璃棒搅拌漏斗中的液体以加快过滤的速度 |
| D.加入盐酸以除去硫酸钠中的少量碳酸钠杂质 |
10、能源可划分为一级能源和二级能源,自然界直接提供的能源为一级能源,需要消耗其它能源的能量间接获取的能源称为二级能源。下列关于能源的说法正确的是
C.电能是一级能源 D.煤气是一级能源
下列关于化学键的说法正确的是
| A.构成单质分子的微粒一定含有共价键 |
| B.由非金属元素组成的化合物不一定是共价化合物 |
| C.金属元素与非金属元素形成的化学键一定是离子键 |
| D.不同元素组成的多原子分子里的化学键一定是极性键 |
下列各装置中,能构成原电池的是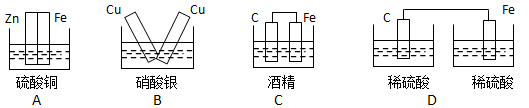
下列叙述中,正确的是
| A.39K+和40Ca2+微粒中的电子数不相等而中子数相等 |
| B.D2和He在同温同压时,若体积相等,则质量相等 |
| C.同一元素的各种同位素的物理性质、化学性质均相同 |
| D.两个质子数和电子数都相等的微粒一定是同种元素 |
下列说法不正确的是
| A.化学反应除了生成新物质外,一定伴随着能量变化 |
| B.需要加热才能发生的反应不一定是吸热反应 |
| C.焓变的符号是△H,单位是kJ/mol,反应热的单位是kJ |
| D.化学反应的实质是旧键断裂和新键生成 |