在硫化氢的水溶液中,存在以下平衡:H2S HS-+H+、HS-
HS-+H+、HS- H++S2-,若使溶液的pH减小,则c(S2-)
H++S2-,若使溶液的pH减小,则c(S2-)
| A.增大 | B.减小 | C.不变 | D.可能增大也可能减小 |
下列各组离子,在溶液中能大量共存、加入NaOH溶液后加热既有气体放出又 有沉淀生成的一组是
有沉淀生成的一组是
A.Ba2+、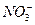 、 、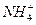 、 、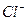 |
B.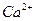 、 、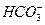 、 、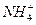 、 、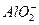 |
C.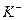 、Ba2+、 、Ba2+、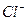 、 、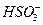  |
D.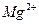 、 、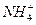 、 、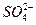 、 、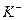 |
为了检验某含有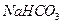 杂质的
杂质的 样
样 品的纯度,现将
品的纯度,现将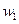 克样品加热,其质量变为
克样品加热,其质量变为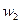 g,,则该样品的纯度(质量分数)是
g,,则该样品的纯度(质量分数)是
A.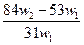 |
B. |
C.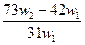 |
D.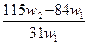 |
在一密闭容器中进行如下反应:2SO2(g) +O2(g) 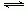 2SO3(g) ,已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
2SO3(g) ,已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
| A.SO2为0.4mol/L、O2为0.2mol/L | B.SO2为0.25mol/L |
C.SO2 、SO3均为0.15mol/L 、SO3均为0.15mol/L |
D.SO3为0.4mol/L |
下列叙述正确的是
| A.构成分子晶体的粒子中一定含有共价键 |
| B.在离子晶体中不可能存在非极性键 |
| C.离子化合物中可能含有共价键 |
| D.在原子晶体中不可能存在极性共价键 |
含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
| A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl- |
| B.x=0.6a,2Br-+ Cl2=Br2+2Cl- |
| C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- |
| D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl- |