下列有关NaHCO3与Na2CO3的说法中,正确的是
| A.分别加热两种样品,没有残留物质是NaHCO3 |
| B.分别配成溶液,再加入石灰水,无白色沉淀生成的是NaHCO3 |
| C.分别与相同物质的量浓度的盐酸反应,产生CO2的速率Na2CO3<NaHCO3 |
| D.二者在一定条件下不能相互转化 |
实验是化学研究的基础,关于下列各装置图的叙述中,正确的是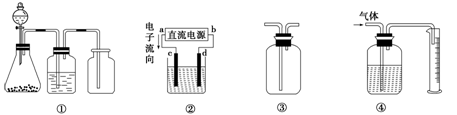
| A.装置①是一套实验室制气装置,用于发生、干燥和收集气体,如铜屑与稀硝酸反应制取气体 |
| B.装置②中,a为正极,d为阳极 |
| C.装置③可用于收集H2、NH3、Cl2、HCl、NO2等 |
| D.装置④能用于测量气体体积 |
下列有关晶体的叙述中错误的是
| A.石墨的层状结构中由共价键形成的最小的碳环上有六个碳原子 |
| B.氯化钠晶体中每个Na+周围紧邻的有6个Cl— |
| C.CsCl晶体中每个Cs+周围紧邻的有8个Cl—,每个Cs+周围等距离紧邻的有6个Cs+ |
| D.在面心立方最密堆积的金属晶体中,每个金属原子周围紧邻的有4个金属原子 |
下面的排序不正确的是
| A.晶体熔点由低到高:CF4<CCl4<CBr4<CCI4 |
| B.硬度由大到小:金刚石>碳化硅>晶体硅 |
| C.熔点由高到低:Na>Mg>Al |
| D.晶格能由大到小:NaF> NaCl> NaBr>NaI |
3—甲基戊烷的一氯代产物有(不考虑立体异构)
| A.3种 | B.5种 | C.4种 | D.6种 |
下列叙述中正确的是
| A.只含离子键的化合物才是离子晶体 |
| B.(NH4)2SO4晶体是含有离子键、极性共价键和配位键的晶体 |
| C.由于I—I中的共价键键能比F—F、Cl—Cl、Br—Br都弱,因此在卤素单质中I2的熔点、沸点最低 |
| D.液态氯化氢能导电,说明氯化氢不是共价化合物 |