某含铬(Cr2O72-)废水用硫酸亚铁铵废水用硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀经干燥后得到n molFeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述错误的是
| A.消耗硫酸亚铁铵的物质的量为n(2-x)mol |
| B.处理废水中Cr2O72-的物质的量为nx/2mol |
| C.反应中发生转移的的电子数为3nx NA |
| D.在FeO·FeyCrxO3中,3x=y |
下列物质的电离方程式不正确的是
A.NaHCO3===Na++H++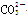 |
B. |
| C.AlCl3===Al3++3Cl- |
D.NaHSO4===Na++H++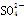 |
下列说法中正确的是
| A.胶体中分散质粒子直径小于1×10-9m |
| B.区别胶体与溶液的最简单的方法是丁达尔效应 |
| C.往NaOH溶液中滴入FeCl3溶液立即可制得胶体 |
| D.用半透膜分离胶体和悬浊液 |
已知1L 0.1 mol/L的NaRO3溶液中含RO3-的质量为8.5克。在RO3-中,氧原子中质子数和中子数相等,R的中子数为20,则RO3-的核外电子总数为
| A.40 | B.42 | C.44 | D.46 |
某溶液中仅含有Na+、Mg2+、SO42-、Cl-四种离子,其物质的量浓度比为c(Na+)∶c(Mg2+)∶c(Cl-)=3∶4∶5,若Na+的物质的量浓度为3 mol·L-1,则SO42-的物质的量浓度为
| A.2 mol·L-1 | B.3 mol·L-1 |
| C.4 mol·L-1 | D.8 mol·L-1 |
实验室用固态不纯氯化钠(含少量泥沙和Na2SO4杂质)制取纯净氯化钠溶液。下列操作可供选用:①逐滴加入稀盐酸至稍过量;②煮沸;③加蒸馏水溶解;④过滤
⑤加入稍过量的Na2CO3溶液;⑥加入稍过量的BaCl2溶液。上述实验操作的正确顺序应是
| A.①②③④⑤⑥ | B.④③⑥⑤①② |
| C.③⑥⑤④①② | D.③⑥⑤①④② |