【2015年浙江省湖洲市】黄铁矿矿石的主要成分为二硫化亚铁(FeS2),取一块质量为30克的黄铁矿矿石样品在氧气中完全灼烧后得到10克氧化铁(其中的铁全来自二硫化亚铁)同时生成二氧化硫。
(1)二硫化亚铁中硫元素的化合价为
(2)计算黄铁矿矿石样品中二硫化亚铁的质量分数。
2015年5月中国自主知识产权抗癌新药"西达苯胺"全球上市。我国有了自己原创的抗癌新药。某种西达苯胺(化学式为C 22H 19FN 4O 2)药片中,除了含有西达苯胺外,还含有淀粉。
(1)西达苯胺的相对分子质量为 。
(2)药厂检验室对该西达苯胺药片进行检验,若测得药片中氟元素的含量为  ,则该药片中西达苯胺的质量分数是多少?
,则该药片中西达苯胺的质量分数是多少?
小苏打是发酵粉的主要成分之一,可用于制作发面食品。一化学兴趣小组对某小苏打样品中各成分的含量做了如下测定:将一定质量的该样品(已知杂质只含NaCl)加水全部溶解后,得到104.4g溶液,向该溶液中逐渐加入稀盐酸,产生的气体与加入稀盐酸的质量关系如图所示。试计算:
(1)m的值为 。
(2)当恰好完全反应时,所得溶液的溶质质量分数为3%,求原小苏打样品中NaHCO 3与NaCl的质量比 。

小兰进行水的电解实验时,在水中加入少许硫酸钠以增强导电性。她将2.7g硫酸钠固体加入52.7g水中充分溶解,倒入电解器中通电,当正极产生4.8g氧气时结束实验。忽略气体在水中的溶解,请计算(写出计算过程):
(1)负极产生氢气的质量;
(2)实验结束时所得溶液的溶质质量分数。
诺贝尔生理学和医学奖的一次重大失误是1948年授予了瑞士化学家米勒,他发明的剧毒有机氯杀虫剂DDT (化学式C 14H 9Cl 5)带来了许多环境问题,后来被禁用。试计算:
(1)一个DDT分子是由 个原子构成;
(2)DDT中碳元素和氢元素的质量比为 (填最简整数比)。
氧化钴(CoO)溶于盐酸可得到粉红色的氯化钴(CoCl 2)溶液。CoCl 2含结晶水数目不同而呈现不同颜色。利用蓝色的无水CoCl 2吸水变色这一性质可制成变色水泥和显隐墨水。如图是粉红色的六水氯化钴晶体(CoCl 2•6H 2O)受热分解时,剩余固体质量随温度变化的曲线。
已知:①CoCl 2•6H 2O的相对分子质量为CoCl 2和6个结晶水的相对分子质量之和。
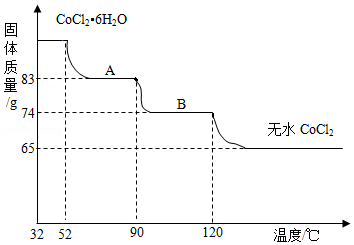
②CoCl 2•6H 2O受热分解完全脱水的化学方程式为:CoCl 2•6H 2O 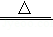 CoCl 2+6H 2O。
CoCl 2+6H 2O。
请回答:
(1)CoCl 2的钴元素的化合价为 价。
(2)求物质A(CoCl 2•xH 2O)中的x值。